
| A. | 8.1g | B. | 3.6g | C. | 4.05g | D. | 2.7g |
分析 铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,若Al都完全反应,则生成氢气应相等,而应结束后测得生成的气体体积比为甲:乙=2:3,由方程式:2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,可知相同物质的量的Al反应时,消耗HCl较多,故酸与金属反应时酸不过量,碱与金属反应时碱过量,结合方程式计算解答.
解答 解:铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,若Al都完全反应,则生成氢气应相等,而应结束后测得生成的气体体积比为甲:乙=2:3,由方程式:2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,可知相同物质的量的Al反应时,消耗HCl较多,可知酸与金属反应时酸不过量,碱与金属反应时碱过量,
盐酸和氢氧化钠溶液中溶质的物质的量均为0.2L×3mol/L=0.6mol,
设铝与酸反应时酸完全反应,生成的氢气的物质的量为x,则:
2Al+6HCl═2AlCl3+3H2↑
6 3
0.6 0.3
则:n(H2)=0.3mol,
则碱与金属铝反应生成的氢气的物质的量为0.3mol×$\frac{3}{2}$=0.45mol,
碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为y,则:
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
0.3 0.45
则:n(Al)=0.3mol,
则铝的质量为0.3mol×27g/mol=8.1g,
故选A.
点评 本题考查化学反应方程式的计算,涉及过量计算问题,关键是判断反应中酸、碱是否足量,难度中等.


科目:高中化学 来源: 题型:选择题
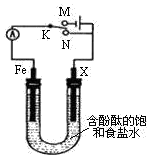
| A. | 电键K置于N处,若X为铜棒,可实现铁棒免受腐蚀 | |
| B. | 电键K置于N处,若X为锌棒,铁棒上发生的电极反应式为O2+2H2O+4e-═4OH- | |
| C. | 电键K置于M处,若X为碳棒,碳棒附近溶液变红 | |
| D. | 电键K置于M处,若X为铜棒,可实现在铁棒上镀铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2有毒,可以用作某些食品防腐剂 | |
| B. | 铅笔芯的原材料为铅,儿童使用时如果用嘴吮吸能够引起铅中毒 | |
| C. | 双氧水是绿色氧化剂,可作医疗消毒剂,说明H2O2对人体无害 | |
| D. | 科学家推测月尘[即月球上直径小于10μm(1μm=1×10-6m)的浮尘]是“玉兔号”出现控制异常情况的主要原因,月尘分散在空气中形成的分散系属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在烷烃分子中,可能会有碳碳双键 | |
| B. | 烷烃中除甲烷外,很多都能使紫色KMnO4溶液褪色 | |
| C. | 分子通式为CnH2n+2的烃不一定是烷烃 | |
| D. | 所有的烷烃在光照条件下都能与氯气发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及现象 | 结论 |
| A | 测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,前者pH比后者的大 | 非金属性:S>C |
| B | 向苯酚浊液中滴加Na2CO3溶液,浊液变澄清 | CO32-结合质子能力比C6H5O-弱 |
| C | 向10mL 0.2mol•L-1NaOH溶液中滴入2滴0.1mol•L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol•L-1FeCl3溶液,白色沉淀转化为红褐色沉淀 | 相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色 | Fe3+的氧化性大于I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | 90℃时,测得纯水中c(H+)•c(OH-)=3.8×10-13:H2O(l?)H+(aq)+OH-(aq)△H<0 | |
| C. | 氨水中滴入酚酞溶液.溶液变红:NH3•H2O═NH4++OH- | |
| D. | 向澄清石灰水中通入过量CO2,溶液变浑浊:Ca2++CO2+2OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
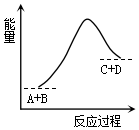
| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 该反应只有在加热条件下才能进行 | |
| C. | 该反应为放热反应 | |
| D. | 该反应为吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com