
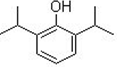
 丙泊酚,其化学名为2,6-双异丙基苯酚,是目前临床上普遍用于麻醉诱导、麻醉
丙泊酚,其化学名为2,6-双异丙基苯酚,是目前临床上普遍用于麻醉诱导、麻醉| A. | 分子式为C10H20O | |
| B. | 分子中所有碳原子可能在同一平面中 | |
| C. | 该物质的1H核磁共振谱图中有5个特征峰,峰值强度比大概为:1:1:2:2:12 | |
| D. | 该物质结构中有2个手性碳原子 |
分析 由结构简式可确定有机物分子式,有机物含有酚羟基,具有苯环的性质,结合同系物的定义以及碳原子的成键特点判断分子的空间构型.
解答 解:A.由结构简式可知分子式为C12H18O,故A错误;
B.分子中含有饱和烃基,具有甲烷的结构特点,则所有碳原子不可能都在同一平面上,故B错误;
C.丙泊酚是左右对称结构,共有5种氢原子,个数分别为1、1、2、2、12,所以核磁共振谱图中有5个特征峰,峰值强度比大概为1:1:2:2:12,故C正确;
D.手性碳原子是连有四个不同基团的碳原子,该物质中不存在手性碳原子,故D错误;
故选C.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力考查,有利于培养学生的良好的科学素养,注意把握有机的组成、结构和性质,难度不大.


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子. ;ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑.
;ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂在空气中完全燃烧转化为水和二氧化碳 | |
| B. | 聚氯乙烯塑料强度大,抗腐蚀性强,可以用来包装需长时间保存的食品 | |
| C. | 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 | |
| D. | 用于食品包装的塑料制品,属于热塑性塑料,可回收再利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,反应类型为取代反应.
,反应类型为取代反应.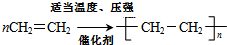
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
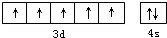 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com