
分析 铵根离子与氢氧根离子反应生成一水合氨,铝离子与氢氧根离子反应生成氢氧化铝沉淀,碱过量时氢氧化铝与氢氧根离子反应生成偏铝酸根离子和水,镁离子与氢氧根离子反应生成氢氧化镁沉淀,硫酸根离子与钡离子反应生成硫酸钡沉淀,据此写出反应的离子方程式.
解答 解:NH4+、Al3+、Mg2+、SO42-中逐滴加入NaOH溶液或Ba(OH)2溶液,发生反应的离子方程式有:NH4++OH-=NH3•H2O,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,Mg2++2OH-=Mg(OH)2↓,SO42-+Ba2+=BaSO4↓,
故答案为:NH4++OH-=NH3•H2O,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,Mg2++2OH-=Mg(OH)2↓,SO42-+Ba2+=BaSO4↓.
点评 本题考查了离子方程式的书写方法,为高考的高频题,题目难度不大,明确离子反应发生条件为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的灵活应用能力.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | H2SO4>NO2>O2 | B. | O2>SO3>H2SO4 | C. | NO2>O2>SO3 | D. | O2>NO2>SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
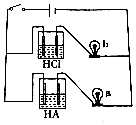
| A. | HA属于弱酸 | |
| B. | pH=1的HA溶液中由水电离出的c(H+)=10-13•L-1 | |
| C. | 等体积、等pH的HA和HCl溶液分别和NaOH溶液反应,HA消耗的NaOH较多 | |
| D. | 等体积的上述两种酸溶液分别和NaOH溶液反应,HA消耗的NaOH较少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 实验室用如图所示的装置进行中和热测定实验.下列说法正确的是( )
实验室用如图所示的装置进行中和热测定实验.下列说法正确的是( )| A. | 用强酸和弱碱进行实验,测定的中和热(△H)一定为-57.3kg/mol | |
| B. | 实验过程中,将50mL 0.55mol/L的NaOH溶液逐滴加入到50mL 0.5mol/L的盐酸中 | |
| C. | 实验前用温度计先测量盐酸温度,再用该温度计直接测量NaOH溶液的温度 | |
| D. | 该实验需要计算生成水的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若硝酸有剩余,溶液中存在的金属阳离子有Fe2+、Cu2+ | |
| B. | 若硝酸有剩余,溶液中存在的金属阳离子可能是Fe3+、Cu2+ | |
| C. | 若金属与硝酸均无剩余,溶液中存在的金属阳离子有Fe3+、Fe2+、Cu2+ | |
| D. | 若金属有剩余,剩余金属中一定有铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 爱氏试剂(由质量分数为25%盐酸、96%乙醇与无水乙醚以体积之比为1:3:1配成的混合溶液)是工商部分用于检验猪肉(含N元素)是否变质(如图)的试剂,若观察到有白烟出现,则说明猪肉已变质.下列有关说法正确的是( )
爱氏试剂(由质量分数为25%盐酸、96%乙醇与无水乙醚以体积之比为1:3:1配成的混合溶液)是工商部分用于检验猪肉(含N元素)是否变质(如图)的试剂,若观察到有白烟出现,则说明猪肉已变质.下列有关说法正确的是( )| A. | 白烟的成分为NH4Cl | |
| B. | 可用稀硫酸代替盐酸 | |
| C. | 腐败肉样释放出的是N2 | |
| D. | 该检验可直接将肉样放入爱氏试剂中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
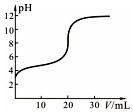 25℃时,用0.1000mol•L-1 KOH溶液滴定20.00mL 0.1000mol•L-1 CH3COOH溶液,滴定中pH变化如图,下列关系错误的是( )
25℃时,用0.1000mol•L-1 KOH溶液滴定20.00mL 0.1000mol•L-1 CH3COOH溶液,滴定中pH变化如图,下列关系错误的是( )| A. | V=0.00 mL时,CH3COOH溶液pH=3,其电离平衡常数K≈10-5mol•L-1 | |
| B. | V=10.00 mL时,溶液中c(CH3COO-)>c(K+)>c(H+)>c(OH-) | |
| C. | 溶液pH=7时,$\frac{c({K}^{+})•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}$=1 | |
| D. | V≥20.00 mL时,溶液中c(K+)=c(CH3COO-)+c(OH-)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用纯铜作阳极、粗铜作阴极 | |
| B. | 电解液的成分保持不变 | |
| C. | 屯解过程中,阳极质量的减少与阴明极质量的增加相等 | |
| D. | 阴极电极反应为:Cu2++2e-=Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com