
【题目】内锌矿的主要成分为ZnS,含有杂质PbS、CuS、FeS、SiO2等,以闪锌矿制备氯化锌的流程如图所示。

请回答下列问题:
(1)配制氯化铁浸渍液时要求pH为0.8~1之间,pH太高则 ,pH太低,浸渍矿石会产生有害气体 ,操作①是 。由氯化锌溶液制备氯化锌晶体的方法是 。
(2)高沸点溶剂R—4E几乎不溶于水,120℃时硫在R—4E里的溶解度为365g,室温时溶解度为35.9g,从浸出液B提取硫的方法是 。硫是工业制备硫酸的原料,现有1吨矿石,硫的总含量为24%,最多制备浓度98%的硫酸 吨。
(3)氯化铁与硫化锌发生反应:![]() ,则氯化铁与FeS反应的方程式为 。
,则氯化铁与FeS反应的方程式为 。
(4)溶液X的成分的化学式为 ,该流程中循环使用的物质是 。
(5)由氯化亚铁溶液制备氯化铁溶液,可以用![]() 、
、![]() ,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。
,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。
【答案】
(1)铁离子会水解;硫化氢;过滤;加入盐酸再蒸发;
(2)冷却饱和溶液;0.75;
(3)2FeCl3+FeS═3FeCl2+S;
(4)ZnCl2、FeCl2;溶剂R-4E、有机萃取剂TBP、氯化铁溶液;
(5)4Fe2++4H++O2![]() 4Fe3++2H2。
4Fe3++2H2。
【解析】
试题分析:(1)因为铁离子会水解呈酸性,所以配制氯化铁浸渍液时要求pH为0.8~1之间,防止铁离子水解,矿石的主要成份为硫化物,溶液pH太低,会产生硫化氢气体,分离固体和液体一般用过滤操作,由氯化锌溶液制备氯化锌晶体时,要防止锌离子水解产生氢氧化锌,所以操作的方法是加入盐酸再蒸发,故答案为:铁离子会水解;硫化氢;过滤;加入盐酸再蒸发;
(2)根据题中数据,硫在R-4E里的溶解度受温度影响较大,所以从浸出液B提取硫的方法是冷却饱和溶液,1吨矿石,硫的总含量为24%,所以硫元素的质量为0.24t,根据硫元素守恒可知,可制备浓度98%的硫酸的质量为![]() ×98t=0.75t,故答案为:冷却饱和溶液;0.75;
×98t=0.75t,故答案为:冷却饱和溶液;0.75;
(3)根据氯化铁与硫化锌发生反应:2FeCl3+ZnS═ZnCl2+2FeCl2+S可知,氯化铁与FeS反应,铁离子能氧化-2价的硫生成硫单质,反应的方程式为2FeCl3+FeS═3FeCl2+S,故答案为:2FeCl3+FeS═3FeCl2+S;
(4)根据上面的分析可知,溶液X的成分的化学式为ZnCl2、FeCl2,该流程中循环使用的物质是溶剂R-4E、有机萃取剂TBP、氯化铁溶液,故答案为:ZnCl2、FeCl2;溶剂R-4E、有机萃取剂TBP、氯化铁溶液;
(5)酸性条件下,使用催化剂在50℃左右通入氧气可将亚铁离子氧化成铁离子,反应的离子方程式为4Fe2++4H++O2![]() 4Fe3++2H2O,故答案为:4Fe2++4H++O2
4Fe3++2H2O,故答案为:4Fe2++4H++O2![]() 4Fe3++2H2。
4Fe3++2H2。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】图中的实验装置可用于制取乙炔。请填空:


(1)图中,A管的作用是 。制取乙炔的化学方程式是 。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 ,乙炔发生了 反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象是 , 乙炔发生了 反应。
(4)为了安全,点燃乙炔前应 ,乙炔燃烧时的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中的两种组成。常温下,甲是一种含氮质量分数为87.5%的液态化合物,其相对分子质量与空气中某种主要成分的相对分子质量相等;乙和丙是铜的两种常见氧化物,乙是新制氢氧化铜与乙醛反应的还原产物。试回答下列问题:
(1)甲的结构式 。
(2)甲是一种二元弱碱,则甲与过量硫酸反应的产物为 (写化学式)。
(3)甲和丙反应的产物中含有乙和一种气态单质,写出其化学方程式 。
(4)向乙的固体中加入过量硫酸酸化的硫酸铁溶液,乙固体完全溶解,得到透明溶液。写出其离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别由C、H、O三种元素组成的有机物A、B、C互为同分异构体,它们分子中C、H、O元素的质量比为15:2:8,其中化合物A的质谱图如图.
A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1:1:2,它能够发生银镜反应.B为五元环酯.C的红外光谱表明其分子中存在甲基.其它物质的转化关系如下:
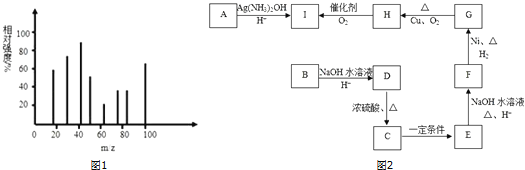
(1)A的分子式是: .
(2)B和G的结构简式分别是: 、 .
(3)写出下列反应方程式(有机物用结构简式表示)
D→C ;
H→G .
(4)写出由单体F发生缩聚反应生成的产物的结构简式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构和元素周期律的表述正确的是
A. 氮的非金属性比磷强,所以氮气的性质比白磷活泼
B. ⅦA族元素一定是同周期中非金属性最强的元素
C. IA族元素的金属性一定比IIA族元素的金属性强
D. Na+半径大于Cl﹣半径
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联苄(![]() )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
(一)催化剂的制备:下图是实验室制取少量无水AlCl3的相关实验装置的仪器和药品:

(1)将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d接e,_______接_______,_________接________,_________接________。
(2)有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl3。你认为这样做是否可行__________(填“可行”或“不可行”),你的理由是________________。
(3)装置A中隐藏着一种安全隐患,请提出一种改进方案:_____________。
(二)联苄的制备
联苄的制取原理为:![]()
反应最佳条件为n(苯) :n(1,2-二氯乙烷)=10 :1,反应温度在60-65℃之间。
实验室制取联苄的装置如下图所示(加热和加持仪器略去):
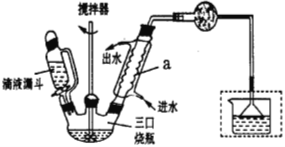
实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7 mL1,2-二氯乙烷,控制反应温度在60-65℃,反应约60min。将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2 g。
相关物理常数和物理性质如下表
名称 | 相对分子质量 | 密度/(gcm-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
1,2-二氯乙烷 | 99 | 1.27 | -35.3 | 83.5 | 难溶水,可溶苯 |
无水氯化铝 | 133.5 | 2.44 | 178(升华) | 遇水水解,微溶苯 | |
联苄 | 182 | 0.98 | 52 | 284 | 难溶水,易溶苯 |
(4)仪器a的名称为______________,和普通分液漏斗相比,使用滴液漏斗的优点是_________。
(5)洗涤操作中,水洗的目的是_____________;无水硫酸镁的作用是______________。
(6)常压蒸馏时,最低控制温度是________________。
(7)该实验的产率约为______________。(小数点后保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是( )
A.SO2和FeSO4溶液使酸性高锰酸钾的紫色褪去
B.浓硫酸和浓盐酸长期暴露在空气中浓度降低
C.不能用pH试纸测定浓硫酸和新制氯水的pH
D.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图判断,下列说法正确的是( )

A. 装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-Fe2+
B. 装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e-4OH-
C. 装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D. 放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com