
【题目】Al-Ag2O电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则下列说法错误的是 ( )
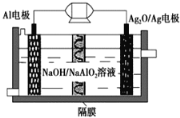
A. 工作时正极发生还原反应,且正极质量逐渐减小
B. 当电极上生成1.08 g Ag时,电路中转移的电子为0.01 mol
C. Al电极做负极,电极反应式为:Al-3e-=Al3+
D. 工作时电解液中的Na+移向Ag2O/Ag电极
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、Ag+、NO3-、Cl-B.Na+、Cu2+ 、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl-D.K+、Ba2+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:

(1)写出下列元素名称:②_________;___________。
(2)在这些元素中,金属性最强的元素是______(用元素符号表示),元素⑨与元素⑩相比,非金属性较强的是___________(用元素符号表示)。下列表述中能证明这一事实的是______________。
a.常温下⑨的单质和⑩的单质状态不同
b. ⑩的氢化物比⑨的氢化物稳定
c.一定条件下⑨和⑩的单质都能与氢氧化钠溶液反应
(3)⑦的最高价氧化物对应水化物与⑩的最高价氧化物对应水化物反应的离子方程式为:______。
(4)②的气态氢化物与HC1在空气中相遇有白烟生成,写出白烟对应物质的电子式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质子数≤18的A和M两种元素,已知A2﹣与M+的电子数之差为8,则下列说法正确的是( )
A.A和M原子的最外层电子数之差不一定为5
B.A和M原子的最外层电子数之和一定为7
C.A和M原子的电子数之差一定为11
D.A和M的原子序数之差不一定为5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味、遇水反应生成一种氯化物和两种氮化物。某学习小组在实验空用Cl2和NO制备ClNO并测定其纯度,相关实验装置(夹持装置略去)如下图所示。请回答:

(1)制备C12发生装置可以选用____(填写字母代号),请写出发生反应的离子方程式:____________。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→_______(按气流方向,用小写字母表示)。
(3)实验室可用下图装置制备亚硝酰氯(C1NO):
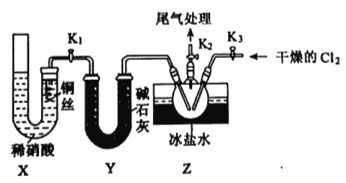
①实验室也可用B装置制备NO,X装置的优点为__________。
②检验装置气密性并装入药品,打开K2,然后再打开K1,通入一段时间气体,其目的为_______,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中C1NO可能发生反应的化学方程式为________。
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmolL-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(C1NO)的质量分数为______(用代数式表示)。[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(K2CrO4)=1×10-12]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B均为短周期元素中的一种,已知A的原子序数为n,A2+离子比B2-离子少8个电子,则B的原子序数为
A. n+4B. n+6C. n+8D. n+10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2和H2合成NH3的能量变化如图所示,该反应的热化学方程式是( )
A.N2(g)+3H2(g)2NH3(g);△H=2(b﹣a) kJ/mol
B.N2(g)+3H2(g)2NH3(l);△H=2(a﹣b﹣c) kJ/mol
C.![]() N2(g)+
N2(g)+ ![]() H2(g)NH3(l);△H=(b+c﹣a) kJ/mol
H2(g)NH3(l);△H=(b+c﹣a) kJ/mol
D.![]() N2(g)+
N2(g)+ ![]() H2(g)NH3(g);△H=(a+b) kJ/mol
H2(g)NH3(g);△H=(a+b) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】难挥发性二硫化钽(TaS2)可采用如下装置提纯.将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中.反应如下:TaS2(s)+2I2(g)TaI4(g)+S2(g)下列说法正确的是( )![]()
A.在不同温度区域,TaI4的量保持不变
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象或化学方程式 | 结论 |
A | 取1mL20%的蔗糖溶液,加入适量稀硫酸,水浴加热后取少量溶液,加入几滴新制Cu(OH)2悬浊液,加热 | 溶液中未出现砖红色沉淀 | 蔗糖未水解 |
B | 将C和SiO2的固体混合物高温加热 | 2C+SiO2 | 非金属性:C>Si |
C | 向盛有2mL0.1mol/L的NaCl溶液的试管中逐滴加入几滴0.1mol/L的AgNO3溶液,充分反应后,再逐滴加入0.1mol/L的KI溶液 | 白色沉淀变为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
D | 向待测液中加入适量的稀NaOH溶液,将|湿润的蓝色石蕊试纸放在试管口 | 湿润的蓝色石蕊试纸未变红 | 在待测液中不存在NH4+ |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com