
(17分)如右图所示:

(1)将铜棒和铝棒用导线连接后置于盛稀盐酸的烧杯中,看到的现象是 。铝棒做 极,该极的电极反应方程式为 _______ 。
(2)如果将盐酸换成NaOH溶液,该电池发生的总反应离子方程式为_________________。
此时铝棒做 极,该极的电极反应方程式为 。
(3)如果将盐酸换成浓硝酸溶液,则铝棒做 极。
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
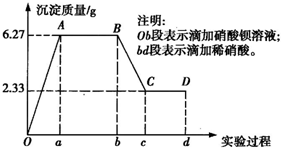 某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO
某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
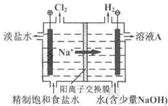 (2011?北京)氯碱工业中电解饱和食盐水的原理示意图如右图所示.
(2011?北京)氯碱工业中电解饱和食盐水的原理示意图如右图所示.
| ||
| ||
 HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出 HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
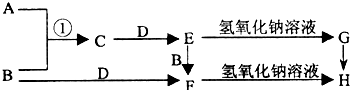
查看答案和解析>>
科目:高中化学 来源: 题型:
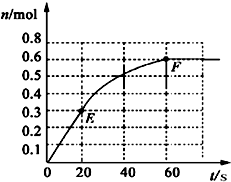 373K时,某1L密闭容器中加入1molPCl5发生如下可逆反应:
373K时,某1L密闭容器中加入1molPCl5发生如下可逆反应: PCl3(g)+Cl2 (g).其中物质PCl3的物质的量变化如右图所示.
PCl3(g)+Cl2 (g).其中物质PCl3的物质的量变化如右图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
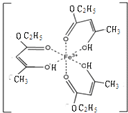 Ⅰ.氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如右图所示.
Ⅰ.氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如右图所示.| A-B | A=B | C-B | C=B | |
| 键能/kJ?mol-1 | 360 | 803 | 464 | 640 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com