
| ||
| ||
 ;
;  ;
;
| ||


科目:高中化学 来源: 题型:
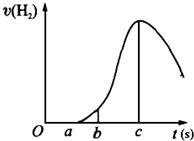 把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:
把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
6 3 |
14 7 |
23 11 |
24 12 |
7 3 |
14 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(ml) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl溶液与NaOH溶液混合:OH-+NH4+═NH3?H2O |
| B、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| C、将铝粉投入氢氧化钠溶液中:Al+2OH-═2AlO2- |
| D、NaHCO3溶液与盐酸混合:HCO3-+H+═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
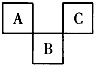 如图是元素周期表短周期的一部分,A、C两种元素的核外电子数之和等于B的核外电子数.下列叙述正确的是( )
如图是元素周期表短周期的一部分,A、C两种元素的核外电子数之和等于B的核外电子数.下列叙述正确的是( )| A、A元素位于第二周期、ⅥA族 |
| B、原子半径C>B>A |
| C、在一定条件下,A、B的气态氢化物都能够与氧气反应 |
| D、三种元素都存在最高价含氧酸,且都显强酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
252 98 |
A、
| ||
B、
| ||
C、
| ||
| D、锎元素位于第6周期 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaN3中只含有离子键 |
| B、1mol NaN3完全分解最多可以产生33.6L N2 |
| C、当有4.2g N2生成时,转移电子数约为6.02×1022 |
| D、常温下,NaN3化学性质稳定,包装盒上无需特别说明注意事项 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com