
| 开始沉淀的PH | 沉淀完全的PH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
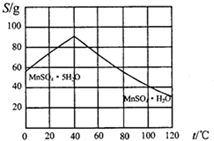
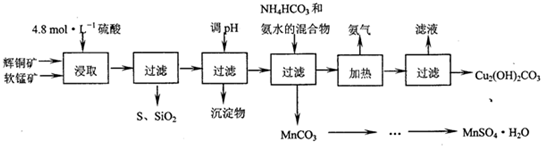
分析 辉铜矿主要成分为Cu2S,软锰矿主要成分MnO2,都含少量Fe2O3、SiO2等杂质,加入稀硫酸浸取,过滤得到SiO2、单质S,滤液中含有Fe3+、Mn2+、Cu2+,用氨水调节溶液pH使铁离子转化为氢氧化铁过滤除去,不会引入新杂质,滤液中加入碳酸氢铵和氨水,使锰离子转化为碳酸锰,碳酸锰再与硫酸反应,经过蒸发结晶得到硫酸锰晶体.过滤得到滤液赶出的氨气可以循环使用,同时得到碱式碳酸铜.
(1)矿石颗粒大小影响反应速率,温度升高反应加快,搅拌也可以提高浸取率;
(2)调节溶液pH目的是除去Fe3+离子,Cu2+、Mn2+不能沉淀;
(3)氨气可以循环利用;
(4)温度过高,碱式碳酸铜为分解,温度过低,会有较多的[Cu(NH3)4]SO4存在;
(5)低于40℃结晶析出MnSO4.5H2O,高于40℃结晶析出MnSO4.H2O,趁热过滤,用酒精洗涤,减少溶解损失,在低温下干燥,防止失去结晶水;
(6)可能洗涤不干净,混有硫酸盐,或者部分晶体失去结晶水等.
解答 解:辉铜矿主要成分为Cu2S,软锰矿主要成分MnO2,都含少量Fe2O3、SiO2等杂质,加入稀硫酸浸取,过滤得到SiO2、单质S,滤液中含有Fe3+、Mn2+、Cu2+,用氨水调节溶液pH使铁离子转化为氢氧化铁过滤除去,不会引入新杂质,滤液中加入碳酸氢铵和氨水,使锰离子转化为碳酸锰,碳酸锰再与硫酸反应,经过蒸发结晶得到硫酸锰晶体.过滤得到滤液赶出的氨气可以循环使用,同时得到碱式碳酸铜.
(1)酸浸时,通过粉碎矿石或者升高温度或者进行搅拌或都增加酸的浓度,都可以提高浸取速率,
故答案为:粉碎矿石、升高温度(或适当增加酸的浓度或搅拌);
(2)调节溶液pH目的是使Fe3+转化为氢氧化铁沉淀而除去,Cu2+、Mn2+不能沉淀,可以用氨水,不会引入新杂质,要除去滤液中的Fe3+离子,溶液pH=3.2使Fe3+离子完全沉淀,溶液pH=4.4时铜离子开始沉淀,故pH范围是3.2≤pH<4.4,
故答案为:3.2≤PH<4.4;使Fe3+转化为氢氧化铁沉淀而除去;
(3)由上述分析可知,NH3可以循环利用,
故答案为:NH3;
(4)温度过高,碱式碳酸铜为分解,温度过低,会有较多的[Cu(NH3)4]SO4存在,都将造成碱式碳酸铜产量减少,
故答案为:碱式碳酸铜产量减少;
(5)低于40℃结晶析出MnSO4.5H2O,高于40℃结晶析出MnSO4.H2O,由硫酸锰溶液制备MnSO4•H2O的实验方案为:蒸发、结晶温度高于40℃,趁热过滤,用酒精洗涤,低温干燥,
故答案为:蒸发、结晶温度高于40℃,趁热过滤,用酒精洗涤,低温干燥;
(6)可能洗涤不干净,混有硫酸盐杂质,或者部分晶体失去结晶水等,导致样品纯度大于100%,
故答案为:混有硫酸盐杂质或者部分晶体失去结晶水.
点评 本题属于化学工艺流程题目,以物质制备为载体,考查物质分离提纯、实验条件控制、信息提取与迁移运用,关键是理解工艺流程,较好的考查学生分析能力、化学实验能力,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 2014年西非国家爆发埃博拉病毒,双氧水、高锰酸钾溶液可以完全杀灭该病毒感染,其消毒原理和漂白粉消毒饮用水相同 | |
| B. | PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,2015年初公益调查《柴静雾霾调查:穹顶之下》发布,引起社会强烈反响,PM2.5引起的雾霾一定属于气溶胶. | |
| C. | 陶瓷、玻璃和光导纤维都是硅酸盐材料 | |
| D. | 原子结构模型的演变经历了: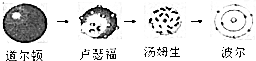 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试剂 温度 | T1/℃ | T2/℃ | T3/℃ |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
温度 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
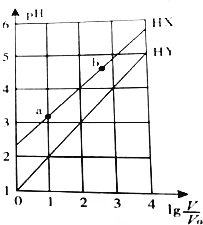
| A. | HX、HY都是弱酸,且HX的酸性比HY的弱 | |
| B. | 常温下,由水电离出的c(H+)•c(OH-):a<b | |
| C. | 相同温度下,电离常数K( HX):a>b | |
| D. | lg$\frac{V}{{V}_{0}}$=3,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),则$\frac{c({X}^{-})}{c({Y}^{-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
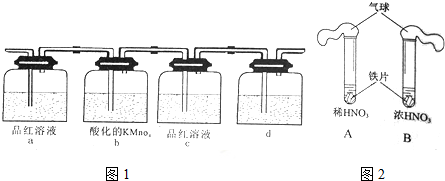
| A. | 在加热条件下能使不活泼金属铜溶解,表现出浓硫酸的强氧化性和酸性 | |
| B. | 可以用铁制或铝制容器贮运,表现出浓硫酸有稳定的化学性质 | |
| C. | 能使胆矾晶体由蓝色变为白色,表现出浓硫酸的脱水性 | |
| D. | 能使蔗糖炭化,表现出浓硫酸的吸水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH+HCl═NaCl+H2O | B. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | ||
| C. | SO3+H2O═H2SO4 | D. | NH4HCO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com