
下列事实不能用有机物分子内基团间的相互作用解释的是( )
A.乙烯能发生加成反应而乙烷不能
B.苯酚能跟NaOH溶液反应而乙醇不能
C.甲苯能使KMnO4酸性溶液褪色而乙烷不能
D.苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可
考点:有机分子中基团之间的关系;烷烃及其命名;乙烯的化学性质;苯的性质;苯的同系物;苯酚的化学性质.
专题:有机物的化学性质及推断.
分析:A.乙烯含有碳碳双键,乙烷属于烷烃,是饱和烃;
B.苯酚能跟NaOH溶液反应而乙醇不能,说明苯基对羟基有影响;
C.苯、乙烷都不能使酸性高锰酸钾褪色,甲苯可以使酸性高锰酸钾褪色,被氧化为苯甲酸,说明苯环对侧链影响;
D.甲苯与硝酸反应更容易,说明甲苯中苯环上H原子更活泼.
解答: 解:A、因为乙烯的结构中含有碳碳双键,能与氢气发生加成反应,而烷烃中则没有,是自身的官能团性质,不是原子团间的相互影响导致的化学性质,故A错误;
B.苯酚可以看作是苯基和羟基连接,乙醇可以可作是乙基和羟基连接,苯酚能跟NaOH溶液反应而乙醇不能,则说明苯基对羟基有影响,故B正确;
C.苯、乙烷都不能使酸性高锰酸钾褪色,甲苯可以使酸性高锰酸钾褪色,被氧化为苯甲酸,说明苯环对侧链影响,故C正确;
D.甲苯与硝酸反应更容易,说明甲基的影响使苯环上的氢原子变得活泼易被取代,故D正确;
故选A.
点评:本题考查有机物结构与性质关系、原子团的相互影响等,难度不大,注意基础知识的把握.


科目:高中化学 来源: 题型:
可逆反应A(g)+3B(g) 2C(g) ΔH=-QkJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 mol A和3 mol B,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2 mol C达到平衡后吸收热量为Q2 kJ;已知Q1=3Q2。下列叙述不正确的是
2C(g) ΔH=-QkJ/mol。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 mol A和3 mol B,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2 mol C达到平衡后吸收热量为Q2 kJ;已知Q1=3Q2。下列叙述不正确的是
A.甲中A的转化率为75% B.Q1+Q2=Q
C.达到平衡后,再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向正向移动
D.乙中的热化学方程式为2C(g) A(g)+3B(g) ΔH= +Q2 kJ/mol
A(g)+3B(g) ΔH= +Q2 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组设计电解饱和食盐水的装置如下图,通电后两极均有气泡产生,下列叙述正确的是( )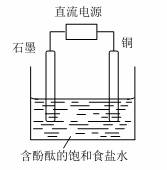
A.铜电极附近观察到黄绿色气体 B.石墨电极附近溶液先变红
C.溶液中的Na+向石墨电极移动 D.铜电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).下列物质中与该产品互为同分异构体的是( )
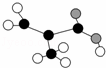
A.CH2═C(CH3)COOH B.CH2═CHCOOCH3
C.CH3CH2CH═CHCOOH D.CH3CH(CH3)COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂鉴别正己烷、1﹣己烯、乙醇、苯酚水溶液4种无色液体,应选用( )
A.酸性KMnO4溶液 B.饱和溴水
C.NaOH溶液 D.AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求回答下列问题:
(1)根据系统命名法,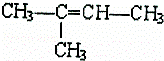 的名称是 :
的名称是 :
(2)乙炔的结构式是 :
(3)顺﹣2﹣丁烯的结构简式是 :
(4)与H2加成生成2,5﹣二甲基己烷的炔烃的结构简式 ;
(5)分子式为C4H100的醇的同分异构体有多种,写出其中能氧化成醛的所有同分异构体的结构简式 :
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A. 元素周期表中位于金属与非金属分界线附近的元素属于过渡元素
B. 短周期第IVA族与VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构
C. C、N、O、H四种元素形成的化合物一定既有离子键又有共价键
D. 第三周期非金属元素含氧酸的酸性从左到右依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤 正确的操作顺序( )
A.①②③⑤④ B.③②①⑤④ C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
用中和滴定法测定烧碱的纯度(烧碱中的杂质不 和酸反应),请根据实验回答:
和酸反应),请根据实验回答:
(1)将称量好的8.8g烧碱样品配制成500mL待测液,配制过程使用的主要仪器除500mL容量瓶、量筒 、烧杯、胶头滴管外,还有一种必须使用的仪器是___________。
、烧杯、胶头滴管外,还有一种必须使用的仪器是___________。
(2)用_______式滴定管量取10.00mL待测液于锥形瓶中,滴入几滴酚酞。
(3)用0.20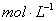 的标准盐酸滴定待测液,判断滴定终点的现象是:_________。
的标准盐酸滴定待测液,判断滴定终点的现象是:_________。
(4)如果实验操作正确,从滴定开始到结束,溶液中的离子浓度关系可以出现的是_______(填答案字母序号)
A. 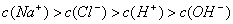
B. 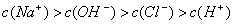
C. 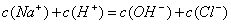
D. 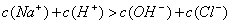
(5)根据下列数据计算,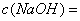 _______mol/L,烧碱的纯度为________%(保留整数)
_______mol/L,烧碱的纯度为________%(保留整数)
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 |
| 20.50 |
| 第二次 | 10.00 | 3.00 | 23.10 |
(6)经过分析发现,本次实验的测定结果比烧碱的实际纯度偏高,造成 误差的可能原因是_________(填答案字母序号,错选此题为0分)
误差的可能原因是_________(填答案字母序号,错选此题为0分)
A. 滴定前平视,滴定后俯视
B. 未用标准液润洗滴定管
C. 用待测液润洗锥形瓶
D. 不小心将标准液滴在锥形瓶外面
E. 滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
F.滴定前尖嘴有气泡,滴定后消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com