
下列性质可以证明某化合物内一定存在离子键的是( )
|
| A. | 可溶于水 | B. | 水溶液能导电 |
|
| C. | 熔融状态可导电 | D. | 熔点350℃ |
考点:
离子化合物的结构特征与性质.
分析:
某种化合物中一定存在离子键,说明该化合物中是离子化合物,离子化合物在熔融状态下能导电,共价化合物在熔融状态下不能导电,据此分析解答.
解答:
解:某种化合物中一定存在离子键,说明该化合物中是离子化合物,离子化合物在熔融状态下能导电,共价化合物在熔融状态下不能导电,
A.可溶于水的化合物可能是共价化合物,如HCl,故A错误;
B.水溶液能导电的化合物可能是共价化合物,如二氧化硫等,故B错误;
C.熔融状态下可导电的化合物中含有自由移动的阴阳离子,所以该化合物的构成微粒是阴阳离子,为离子化合物,一定含有离子键,故C正确;
D.熔点350℃可能是共价化合物,故D错误;
故选C.
点评:
本题考查离子化合物的判断,侧重考查基本概念,明确离子化合物和共价化合物的根本区别是解本题关键,注意不能根据溶解性、电解质溶液酸碱性及导电能力强弱判断离子化合物,为易错点.


科目:高中化学 来源: 题型:
下列说法正确的是( )
A.乙烯、甲苯、苯酚均能与溴水反应
B.乙炔、苯、苯酚均能使酸性高锰酸钾溶液褪色
C.乙醇、苯酚、乙酸都能与氢氧化钠溶液反应
D.乙醇、苯酚、乙酸都能与钠反应,且在相同条件下剧烈程度依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:乙烯是一种无色稍有气味气体,难溶于水,易溶于四氯化碳等有机溶剂:SO2易溶于水,难溶于四氯化碳等有机溶剂.实验室制乙烯时,产生的气体能使溴水褪色,甲、乙同学探究溴水褪色的原因.(气密性已检验,部分夹持装置略).
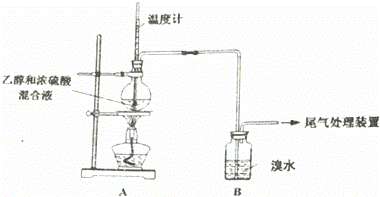
 (1)写出生成乙烯的化学方程式 .烧瓶内液体渐渐变黑说明浓硫酸具有 性.
(1)写出生成乙烯的化学方程式 .烧瓶内液体渐渐变黑说明浓硫酸具有 性.
(2)分析使B中溶液褪色的物质,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,C2H4使B中溶液褪色的化学方程式为 .
②乙根据现象c认为产生了SO2,SO2使B中溶液褪色的化学方程式是 .
(3)为证实各自观点,甲、乙同学重新实验,各自在A、B间增加一个装有某种试剂的洗气瓶,均观察到溴水褪色.
①根据甲的设计,洗气瓶中盛放的试剂是 .
②乙为进一步验证其观点,取少量反应后的B中溶液,加入少量BaCl2溶液,振荡,产生大量白色沉淀,反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各种比较中,正确的是( )
|
| A. | 元素电负性:Ti<Ga |
|
| B. | 第二电离能(I2):Na>Mg |
|
| C. | 金属晶体的晶胞中空间利用率:体心立方堆积>面心立方堆积. |
|
| D. | 晶格能:NaCl>MgO |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A. 化学反应中的能量变化都表现为热量的变化
B. 需要加热才能发生的反应一定是吸热反应
C. 放热反应在常温下一定很容易发生
D. 反应是吸热还是放热必须看反应物和生成物的总能量的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物具有下列性质:能发生银镜反应,滴入石蕊试液不变色,加入少量碱液并滴入酚酞试液,共煮后红色消失。原有机物是下列物质中的( )
A. 甲酸 B. 乙酸甲酯 C. 乙醛 D. 甲酸乙酯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com