
【题目】下列关于晶体与非晶体的说法正确的是( )
A.晶体与非晶体的本质区别在于是否有固定的熔沸点
B.晶体有自范性的原因是粒子在微观空间呈周期有序性排列
C.固体食盐、水晶、塑料、胆矾、玻璃均属于晶体
D.区别晶体与非晶体的最科学可靠的方法是检测其是否具有各向异性
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中进行反应C(s)+H2O(g)![]() CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是

A.5 min时该反应的K值一定小于12 min时的K值
B.0~5 min内,v(H2)=0.05 mol/(L·min)
C.10 min时,改变的外界条件可能是减小压强
D.该反应混合气体的平均相对分子质量:5 min时小于12 min 时的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在指定的环境中一定能大量共存的是( )
A. 在pH为7的溶液中:Ag+、K+、SO![]() 、Cl-
、Cl-
B. 在能使pH试纸变深蓝色的溶液中:Na+、S2-、NO![]() 、CO
、CO![]()
C. 在加入铝粉能产生H2的溶液中:NH![]() 、Fe2+、SO
、Fe2+、SO![]() 、NO
、NO![]()
D. 在由水电离出的c(OH-)=10-13 mol·L-1的溶液中:Na+、Mg2+、Cl-、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A. 1mol醋酸的质量与NA个醋酸分子的质量相等
B. NA个氧分子和NA个氮分子的质量比等于8:7
C. 28g氮气所含的原子数目为NA
D. 在标准状况下,0.5NA个氯气分子所占体积约是11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学反应速率和化学平衡的分析中,不正确的是
①在一密闭容器中充入1 mol H2和1 mol I2,达到平衡后,保持恒压,向其中再加入1 mol H2和1 mol I2,重新达到平衡时,反应速率增大
②已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g) △H<0,升高温度,可以增大正反应速率,减小逆反应速率
2NH3(g) △H<0,升高温度,可以增大正反应速率,减小逆反应速率
③在2 L密闭容器中充入2 mol A气体和1 mol B气体,在一定条件下发生反应:2A(g)+B(g)![]() 2C(g),达到平衡时,C的浓度为0.6 mol/L,则A的转化率为30%
2C(g),达到平衡时,C的浓度为0.6 mol/L,则A的转化率为30%
④Mg、Al在相同条件下分别与0.1 mol/L盐酸反应,反应速率相同
A.①② B.①②③ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业烧碱中常含有少量NaCl。为测定烧碱中NaOH的质量分数,称取1.6g样品与19.00mL、2.0molL—1盐酸恰好反应。
(1)求所消耗盐酸中HCl的物质的量_____________
(2)求工业烧碱中NaOH的纯度_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是 ( )
A.有单质生成的反应一定是氧化还原反应
B.焰色反应是元素表现出来的化学性质
C.由两种元素组成,原子个数比为1:1的物质一定是纯净物
D.能与酸反应产物中有盐和水的氧化物不一定是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.10 | 0.10 | 0.09 |
② | 800 | 0.20 | 0.20 | 0.10 |
③ | 800 | 0.20 | 0. 30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法错误的是
A.实验①中,若5 min时测得n(M) =0.05 mol,则0至5 min时间内,用N表示的平均反应速率v(N) =
0.01 mol/( L·min)
B.实验②中,该反应的平衡常数K=1.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.06
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)工业上将金红石(主要成分TiO2)转化为液态TiCl4,再用金属镁在高温下还原得到金属钛,同时生成MgCl2。
①MgCl2的熔沸点比TiCl4高得多,其原因是______。
②原子半径r(Cl)_____r(Mg),离子半径r(O2-)______r(Mg2+)(填“>”、“<”或“=”)。
(4)金属镍能与CO反应生成一种配合物Ni(CO)4(常温下为无色液体)。Ni(CO)4的固体属于_____晶体,Ni与CO之间的化学键称为__________,提供孤对电子的成键原子是_________。(填元素符号)
(5)一种钛镍合金的立方晶胞结构如图所示:
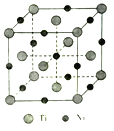
①该合金中Ti的配位数为________。
②若合金的密度为d g/cm3,晶胞边长a=________pm。(用含d的计算式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com