
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 除去CO2气体中的HCl:通过足量的饱和碳酸钠溶液 | |
| B. | 除去NaCl中少量的MgCl2:溶解后,加入过量的NaOH溶液,过滤后向滤液中加适量的盐酸,蒸发结晶 | |
| C. | 除去FeCl2溶液中的FeCl3:加入足量的铜粉,过滤 | |
| D. | 除去Al2O3中的少量SiO2:加入足量的NaOH溶液,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和NaHCO3均可与NaOH溶液反应 | |
| B. | NaHCO3比Na2CO3热稳定性强 | |
| C. | 相同物质的量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体的量相同 | |
| D. | 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,二者消耗的盐酸一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 20% | C. | 15% | D. | 10% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、CO32-、NO3- | B. | NH4+、Na+、SO42-、S2- | ||
| C. | Al3+、Na+、NO3-、I- | D. | CH3COO-、Cl-、Na+、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气在氧气中点燃 | |
| B. | 氮气与氢气在高温高压和有催化剂条件下反应 | |
| C. | 氢氧化钠溶液与盐酸混合 | |
| D. | 二氧化氮与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
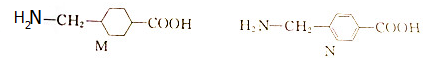
| A. | 1mol M完全燃烧生成6.5mol H2O | B. | CH3CH2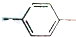 NO2与N互为同分异构体 NO2与N互为同分异构体 | ||
| C. | M、N分子中所有碳原子均共平面 | D. | M、N的核磁共振氢谱均只有5个峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、HCO3-、SO42-、OH- | B. | Na+、Cu2+、Cl-、SO42- | ||
| C. | Na+、H+、CO32-、Cl- | D. | Na+、Mg2+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 室温下,14.0g分子通式为CnH2n烯烃中含有的碳碳双键数目为$\frac{{N}_{A}}{n}$ | |
| C. | 标准状况下,5.6L O2与适量Na加热反应,转移的电子数一定为NA | |
| D. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com