
下列各变化中属于原电池反应的是( )
①在空气中金属铝表面迅速氧化形成保护层,②镀锌铁表面有划损时,仍然能阻止铁被氧化,
③红热的铁丝与冷水接触,表面形成蓝黑色保护层,
④锌与稀硫酸反应时,加入少量CuSO4溶液可使反应加快
A.只有②④ B.只有④ C.只有②③④ D.只有①②④
科目:高中化学 来源: 题型:
下列晶体分类中正确的一组是( )
| 选项 | 离子晶体 | 原子晶体 | 分子晶体 | 金属晶体 |
| A. | NH4Cl | Ar | C6H12O6 | 生铁 |
| B. | H2SO4 | Si | S | Hg |
| C. | CH3COONa | SiO2 | I2 | Fe |
| D. | Ba(OH)2 | 石墨 | 普通玻璃 | Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A.标准状况下,11.2 L Cl2通入含0.5molFeBr2的溶液中转移电子数为1.5NA
B.0.1 mol·L-1的AlCl3溶液与NaOH溶液反应所得产物中含Al为0.1NA
C.足量的Zn与浓硫酸共热可生成标准状况下的气体2.24 L,则参加反应的硫酸为0.4 NA
D.常温常压下,5.6g环丙烷和聚乙烯的混合物中含有的碳原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)  Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:

① 实验Ⅰ中,前5min的反应速率v(CO2)= 。
②下列能判断实验Ⅱ已经达到平衡状态的是 。
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO) =v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如下图所示, b点v正 v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是 。

(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式 ,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH= (溶液电解前后体积的变化忽略不计)。
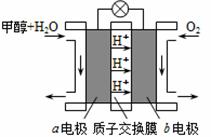
查看答案和解析>>
科目:高中化学 来源: 题型:
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子.若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁.

若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
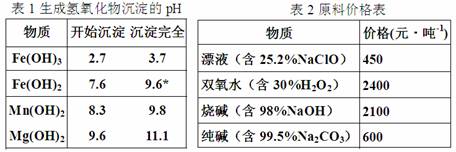
Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去.(1)在步骤②中加入的试剂X,最佳的选择是 ,漂液
其作用是
(2)在步骤③中加入的试剂应是 NaOH
;之所以要控制pH=9.8,其目的是
。
(3)在步骤④中加入的试剂Z应是 纯碱
;
(4)在步骤⑤中发生的反应是 。MgCO3+H2O=Mg(OH)2+CO2
(5)在实验室中,为了除去MgCl2酸性溶液中的Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸,这种试剂是 。
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
(6)已知MgCl2·6H2O受热时发生水解:MgCl2·6H2O=Mg(OH)Cl+HCl↑+5H2O而MgSO4·7H2O受热不易发生水解。试解释原因
。
(7)过滤后的沉淀往往需要洗涤,而选择洗涤沉淀的试剂需要考虑沉淀的损失,例如:分别用等体积的蒸馏水和0.010mol/L硫酸洗涤BaSO4沉淀, 用水洗涤造成BaSO4的损失量大于用稀硫酸洗涤的损失量。试利用平衡移动原理进行解释
。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl- ( )
(2013·海南,10C)
(2)将水蒸气通过灼热的铁粉,铁与水在高温下反应,粉末变红 ( )
(2013·广东理综,23D)
(3)向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含有Fe2+ ( )
(2013·江苏,13D)
(4)Fe3+有氧化性,所以FeCl3溶液可用于回收废旧电路板中的铜 ( )
(2012·广东理综,12D)
(5)在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热 ( )
(2012·浙江理综,8C)
(6)过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液,溶液呈血红色,说明稀HNO3将Fe氧化为Fe3+ ( )
(2011·安徽理综,10A)
(7)Fe在足量Cl2中燃烧生成FeCl2和FeCl3 ( )
(2012·天津理综,2D)
(8)Fe分别与氯气和稀盐酸反应所得氯化物相同 ( )
(2011·重庆理综,7A)
(9)Fe与S混合加热生成FeS2 ( )
(2012·重庆理综,7A)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知:
O2 (g) = O+2(g) + e-  H1= + 1175.7 kJ·mol-1
H1= + 1175.7 kJ·mol-1
PtF6(g) + e- = PtF6-(g)  H2= - 771.1 kJ·mol-1
H2= - 771.1 kJ·mol-1
O2+ PtF6-(s) = O2+(g) + PtF6-  H3= + 482.2 kJ·mol-1
H3= + 482.2 kJ·mol-1
则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)  H=_____________ kJ·mol-1
H=_____________ kJ·mol-1
(2)由C和S形成的液态化合物CS2,0.2mol CS2在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。 该反应的热化学方程式为________。
(3)已知:常温下0.1mol/L的某酸H2A的pH=4,则该酸为 酸(填“强”或“弱”),H2A的电离方程式为 ,该溶液中由水电离出的c(H+)= 。
(4)一定温度下,两种酸:a、盐酸 b、醋酸:
①当两种酸的物质的量浓度相同时,c(H+):a b(填“>”、“<”或“=”,下同)。
②在pH相同、体积相同的两种酸溶液中加入过量的铁粉,反应结束时生成H2的总体积:a b。
③将pH相同,体积相同的两种酸溶液分别加水稀释100倍,所得溶液的pH值:
a b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com