

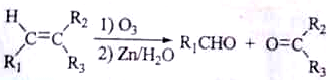

 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O
+H2O
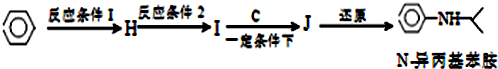
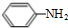 .
. 分析 A的分子式为C6H13Cl,为己烷的一氯代物,在氢氧化钠醇溶液、加热条件下发生消去反应得到B,1mol B发生信息①中氧化反应生成2mol C,且C不能发生银镜反应,B为对称结构烯烃,且不饱和C原子没有H原子,故B为(CH3)2C=C(CH3)2,C为(CH3)2C=O,逆推可知A为(CH3)2CH-CCl(CH3)2;D属于单取代芳烃,其相对分子质量为106,D含有一个苯环,侧链式量=106-77=29,故侧链为-CH2CH3,D为 ,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为
,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为 ,由F的分子式可知,E中硝基被还原为-NH2,则F为
,由F的分子式可知,E中硝基被还原为-NH2,则F为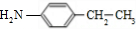 ,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为
,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为 ,据此分析解答.
,据此分析解答.
解答 解:A的分子式为C6H13Cl,为己烷的一氯代物,在氢氧化钠醇溶液、加热条件下发生消去反应得到B,1mol B发生信息①中氧化反应生成2mol C,且C不能发生银镜反应,B为对称结构烯烃,且不饱和C原子没有H原子,故B为(CH3)2C=C(CH3)2,C为(CH3)2C=O,逆推可知A为(CH3)2CH-CCl(CH3)2.D属于单取代芳烃,其相对分子质量为106,D含有一个苯环,侧链式量=106-77=29,故侧链为-CH2CH3,D为 ,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为
,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为 ,由F的分子式可知,E中硝基被还原为-NH2,则F为
,由F的分子式可知,E中硝基被还原为-NH2,则F为 ,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为
,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为 ,
,
(1)A发生消去反应生成B,反应方程式为C(CH3)2Cl-CH(CH3)2+NaOH$→_{△}^{乙醇}$C(CH3)2=C(CH3)2+NaCl+H2O,该反应为消去反应,
故答案为:C(CH3)2Cl-CH(CH3)2+NaOH$→_{△}^{乙醇}$C(CH3)2=C(CH3)2+NaCl+H2O;消去;
(2)D为 ,其名称是乙苯,D发生取代反应生成E,反应方程式为
,其名称是乙苯,D发生取代反应生成E,反应方程式为 +HNO3 $→_{△}^{浓硫酸}$
+HNO3 $→_{△}^{浓硫酸}$ +H2O,
+H2O,
故答案为:乙苯; +HNO3 $→_{△}^{浓硫酸}$
+HNO3 $→_{△}^{浓硫酸}$ +H2O;
+H2O;
(3)通过以上分析知,G结构简式为 ,
,
故答案为: ;
;
(4)B为(CH3)2C=C(CH3)2,其官能团名称是碳碳双键;
若C能发生银镜反应,且1molB同样可以生成2molC,则满足此条件的B的结构简式:CH3CH2CH=CHCH2CH3,
故答案为:碳碳双键;CH3CH2CH=CHCH2CH3;
(5)由苯与浓硝酸、浓硫酸在加热条件下得到H为硝基苯,硝基苯在Fe粉/盐酸条件下还有得到I为 ,再与(CH3)2C=O反应得到
,再与(CH3)2C=O反应得到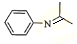 ,最后加成反应还原得到
,最后加成反应还原得到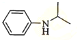 ,
,
故反应条件1所选用的试剂为:浓硝酸、浓硫酸,反应条件2所选用的试剂为:Fe粉/稀盐酸,I的结构简式为  ,
,
故答案为:浓硝酸、浓硫酸;Fe粉/盐酸; .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及信息加工、运用能力,根据反应条件、某些物质分子式结合题给信息进行推断,注意题给信息的灵活运用,题目难度不大.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2做氧化剂,体现氧化性 | |
| B. | NH3做还原剂,体现还原性 | |
| C. | NO为氧化产物 | |
| D. | 该反应中氧化剂和还原剂的质量之比是40:17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
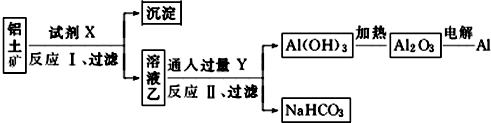
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+ K+ Na+ CO32- NO3- | B. | K+ Na+ Fe2+ SO42- NO3- | ||
| C. | NH4+ K+ Na+ HCO3-[Al(OH)4]- | D. | NH4+ K+ Na+ NO3- I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、Ag+、NO3-、CO32- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Na+、OH-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水能够使石蕊试液变红后褪色,说明氯水中存在H+和漂白性物质 | |
| B. | 向上排空气法收集氯气可以用湿润的KI淀粉试纸是否变蓝检验是否收集满 | |
| C. | 氯水与明矾在自来水处理的过程中原理是不同的 | |
| D. | 实验室应用无色细口玻璃试剂瓶存放保存在煤油中的钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

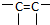 、-COOH
、-COOH ,D的结构简式
,D的结构简式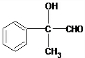 .
.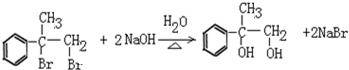
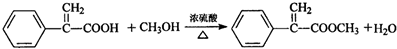
 的同分异构体有多种,写出同时满足:
的同分异构体有多种,写出同时满足: (任写两种).
(任写两种).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com