
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
碳和氮的许多化合物在工农业生产和生活中有重要的作用。
(1)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g) === NH2CO2NH4(s) ∆H=-159.5 kJ·mol-1
②NH2CO2NH4(s) === CO(NH2)2(s)+H2O(g) ∆H=+116.5 kJ·mol-1
③H2O(l) === H2O(g) ∆H=+44.0 kJ·mol-1
则反应2NH3(g)+CO2(g) === CO(NH2)2(s)+H2O(l)的∆H= kJ·mol-1
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2 (g) ∆H=Q kJ·mol-1。
N2(g)+CO2 (g) ∆H=Q kJ·mol-1。
在T1℃时,反应进行到同时间测得各物质的浓度如下;30min后,只改变某一条件,反应重新达到平衡,各物质浓度如图所。
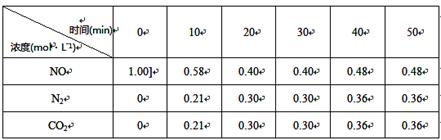
①0~10min内,NO的平均反应速率v(NO)= ,
T1℃时,该反应的平衡常数K= ;
②30min后,只改变某一条件,反应重新达到平衡,各物质浓度如图所示。根据上表中的数据判断改变的条件可能是 (填字母编号)。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂 e.升高温度
③30min后,如果将温度升高至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则 Q 0(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法正确的是
| X | Y | ||
| Z | W | Q |
A.钠与W可能形成Na2W2化合物
B.由Z与Y组成的物质在熔融时能导电
C.W得电子能力比Q强
D.X有多种同素异形体,而Y不存在同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的电子层结构,电子式如图所示: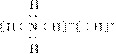 ,下列说法正确的是( )
,下列说法正确的是( )
A.NH5属于离子化合物
B.NH5属于共价化合物
C.NH5只含有离子键
D.NH5只含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是(双选)( )
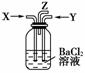
A.洗气瓶中产生的沉淀是碳酸钡
B.在Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2Na[Al(OH)4]+CO2===Na2CO3+2Al(OH)3↓+H2O 2Al(OH)3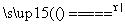 Al2O3+3H2O。某铝合金中含有镁、铜、硅,为了测定该合金中铝的含量,某同学设计如下实验:
Al2O3+3H2O。某铝合金中含有镁、铜、硅,为了测定该合金中铝的含量,某同学设计如下实验:
(1)取样品a g,称取时使用的主要仪器的名称为________。
(2)将样品溶于足量的稀盐酸中,过滤,滤液中主要含有的阳离子(H+除外)有________,滤渣中含有________,在溶解、过滤时,使用的玻璃仪器有____________________________________。
(3)在滤液中加入过量的氢氧化钠溶液,过滤,写出该步操作中有关反应的离子方程式____________________________________,
____________________________________________________。
(4)在第(3)步的滤液中通入二氧化碳,过滤。
(5)将第(4)步的沉淀洗涤数次后,烘干并灼烧至质量不再减少为止,冷却后称量,质量为bg。计算该样品中铝的质量分数是_____。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏________
(填“高”“低”或“无影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏________;若滤渣灼烧不充分,则实验结果偏________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。
反应的化学方程式是________________;样品中铝的质量是________g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是__________________________,氧化铁与铝的质量比是______。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比cb=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com