
【题目】下列变化中,需要加入还原剂的是
A.2Cl—→Cl2B.Fe3+→Fe2+C.NH4+→NH3D.CO32→→CO2
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】科学家预言,燃料电池将是21世纪获得电能的重要途径。
(1)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
①若电解质溶液为KOH,其负极反应为______________________________,电池总反应为 _______________________________。
②若电解质溶液为硫酸,其正极反应为_____________________________,负极反应为________________________________;
(2)近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:

请回答下列问题:
① Pt(a)电极是 _____ 极,电极反应式为_______________________________;
② Pt(b)电极发生________反应(填“氧化”或“还原”)。
③该电池的总反应方程式为_____________________________________________。
④如果该电池工作时电路中通过3 mol电子,则消耗掉的CH3OH有________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是

A. 用图①装置实现铁上镀铜,a 极为铜,电解质溶液可以是CuSO4溶液
B. 图②装置盐桥中 KCl的 Cl-移向乙烧杯
C. 图③装置中钢闸门应与外接电源的负极相连获得保护
D. 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)写出C与酸发生反应的化学方程式是________________。
(2)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①分别写出生成D和F的化学方程式:________________,________________。
②要将NaOH高温熔化,下列坩埚中可选用的是________(填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(3)100 g C与石灰石的混合物充分反应后生成的气体在标况下的体积为11.2 L,100 g混合物中石灰石的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是( )

A. K1闭合,铁棒上发生的反应为2H++2e-→H2↑
B. K1闭合,石墨棒周围溶液pH逐渐升高
C. K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D. K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
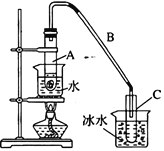
【题目】某化学小组采用类似制乙酸乙酯的装置(如右图所示),用环己醇制备环己烯。
已知: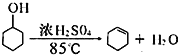
相对分子质量 | 密度/g cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 82 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品
将12.5 mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①在试管中混合环已醇和浓硫酸操作时,加入药品的先后顺序为_________。
②如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_________(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
③将试管C置于冰水中的目的是_______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在__________________层(填“上”或“下”),分液后用__________________(填字母)洗涤。
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
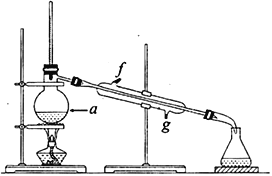
②再将提纯后的环己烯按如图所示装置进行蒸馏。图中仪器a 的名称是_______________。实验中冷却水从__________(填字母)口进入。蒸馏时要加入生石灰,目的是__________________________。
(3)若在制备粗品时环已醇随产品一起蒸出,则实验制得的环己烯精品质量__________(填“高于”、“ 低于”)理论产量。本实验所得到的环已烯质量为6.25g,则产率是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com