

| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
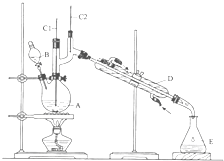 正丁醛是一种化工原料.某实验小组利用如图所示装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图所示装置合成正丁醛.
| ||
| H2SO4 △ |
| 沸点/℃ | 密度/g?cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀醋酸和稀氨水反应 |
| B、稀硫酸和烧碱溶液反应 |
| C、稀盐酸和氢氧化铜反应 |
| D、稀硫酸和氢氧化钡溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略.将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4 L CO2和O2混合气体中含有的氧原子数约为NA |
| B、300 mL 2 mol?L-1蔗糖溶液中所含分子数为0.6 NA |
| C、1 L 1 mol?L-1的K2CO3溶液中离子总数大于3NA |
| D、常温常压下,2.24 L四氯化碳中所含氯原子数约小于0.4 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com