
B.【实验化学】
乙酰苯胺具有退热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称。其制备原理如下:
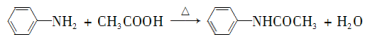
已知:
①苯胺易被氧化;
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
物质 | 熔点 | 沸点 | 溶解度(20 ℃) |
乙酰苯胺 | 114.3 ℃ | 305 ℃ | 0.46 |
苯胺 | -6 ℃ | 184.4 | 3.4 |
醋酸 | 16.6 ℃ | 118 ℃ | 易溶 |
实验步骤如下:
步骤1:在50 mL圆底烧瓶中,加入5 mL苯胺、7.5 mL冰醋酸及少许锌粉,依照下图装置组装仪器。

步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,冷却后抽滤,洗涤,得到粗产品。
请回答下列问题:
(1)步骤1中加入锌粉的作用是____。
(2)步骤2中控制温度计示数约105 ℃的原因是____。
(3)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是____。抽滤装置所包含的仪器除减压系统外还有________、________(填仪器名称)。
(4)步骤3得到的粗产品需进一步提纯,该提纯方法是____。
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,电池放电时时的反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列对电池放电时的分析正确的
A.Pb为正极被氧化 B.电子从PbO2 流向外电路
C.SO42-向PbO2处移动 D.电解质溶液pH不断增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省八市高三教学质量监测考试理科综合化学试卷(解析版) 题型:选择题
X、Y、Z、W是原子序数依次增大的四种短周期主族元素,已知Z的最高正价与最低负价的代数和为4,Y能形成两种常见的液体二元化合物M、Q,其中M是生物生存必需的物质.x能形成多种单质,其中有两种单质硬度差异极大,下列说法中错误的是
A.最高价氧化物对应水化物的酸性:w>Z>x
B.化合物Q中存在两种类型的共价键
C.Z、X都可以形成两种常见的酸性氧化物
D.四种元素的常见单质中X的单质的沸点最高
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:填空题
(17分)KMnO4是常见的试剂。
Ⅰ.某小组拟用酸性KMnO4溶液与H2C2O4(K1=5.4×10-2)的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | 甲 | V(0.010mol/L KMnO4溶液)/mL | M(MnSO4固体)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.0 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
回答下列问题:
(1)完成上述反应原理的离子反应方程式
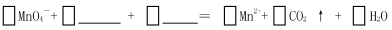
(2)上述实验①②是探究 对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则表格中“甲”应填写 ,a为 ;乙是实验需要测量的物理量,则表格中“乙”应填写 。
(3)上述实验②④是探究催化剂对化学反应速率的影响。
请在答题卷的坐标图中画出实验②和④的能量变化关系图(作必要的标注)。
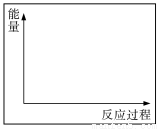
Ⅱ.某化学小组利用下图装置进行实验证明氧化性:KMnO4>Cl2>Br2。限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸
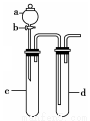
(4)装置a、d中盛放的试剂分别是: 、 ;实验中观察到的现象为 ;此实验装置的不足之处是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如下图所示。已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是
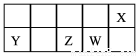
A.X分别与Y、Z形成的化合物中化学键类型相同
B.Z的最高价氧化物的对应水化物酸性比W的强
C.X的简单气态氢化物的稳定性比W的弱
D.原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
(15分)有机物H是一种新型大环芳酰胺的合成原料,可通过以下方法合成:

已知:①苯胺( )有还原性,易被氧化;
)有还原性,易被氧化;
②硝基苯直接硝化主要产物为间二硝基苯。
(1)写出A中含氧官能团的名称:________和________。
(2)写出F的结构简式:________。
(3)步骤④和步骤⑥的目的是____。
(4)写出一种符合下列条件的化合物C的同分异构体的结构简式:____。
①分子中含有2个苯环;
②能与FeCl3溶液发生显色反应;
⑧分子中有3种不同化学环境的氢原子。
(5)对苯二胺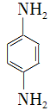 )是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)是一种重要的染料中间体。根据已有知识并结合相关信息,写出以苯、(CH3CO)2O及CH3COOH为主要有机原料制备对苯二胺的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:

查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
一种三室微生物燃料电池污水净化系统原理如右图所示,图中有机废水中有机物可用C6H10O5表示。下列有关说法正确的是
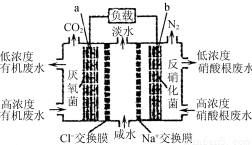
A.b电极为该电池的负极
B.b电极附近溶液的pH减小
C.a电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
D.中间室:Na+移向左室,Cl-移向右室
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河北区高三总复习质量检测一化学试卷(解析版) 题型:选择题
下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+H2O HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
B.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
C.高压比常压有利于合成SO3的反应
D.对CO(g) + NO2 (g)  CO2 (g)+ NO(g) 平衡体系增大压强可使颜色变深
CO2 (g)+ NO(g) 平衡体系增大压强可使颜色变深
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:填空题
(14分)(2010佛山一模)氢化阿托醛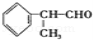 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下: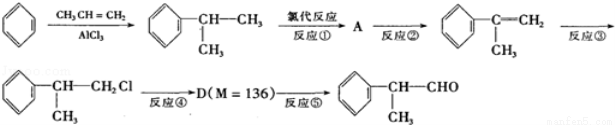
(1)氢化阿托醛被氧化后的含氧官能团的名称是____________.
(2)在合成路线上②③的反应类型分别为②_____________③________________.
(3)反应④发生的条件是_____________________.
(4)由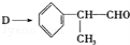 反应的化学方程式为_______________________________
反应的化学方程式为_______________________________
(5)1mol氢化阿托醛最多可和____mol氢气加成,1mol氢化阿托醛发生银镜反应可生成________molAg.
(6)D与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的结构简式为________.D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有______种.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com