
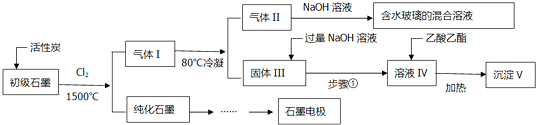
���� ���·�Ӧ��ʯī�����������ʾ�ת��Ϊ��Ӧ���Ȼ���������ʵĺ�����֪������I���Ȼ�����ҪΪSiCl4��AlCl3��FeCl3�ȣ�����I��̼��������ҪΪCO��SiCl4�ķе�Ϊ57.6�棬�����Ȼ���ķе������150�棬80����ȴ�õ����������SiCl4��CO��SiCl4������������Һ��Ӧ�õ����������Ȼ��ƣ���������AlCl3��FeCl3��MgCl2������FeCl3��MgCl2�����������������Һ��Ӧ�õ����������Ȼ��������������������Һ��Ӧ����ƫ�����ƣ����˵õ�����Һ�к���ƫ�����ơ��������������ƣ�����Һ��ƫ�����Ʒ���ˮ�⣬��������������ȥ�������������ƣ��Ҽ���������ˮ��ƽ��һֱ�����ƶ����õ��������������������ơ��Ҵ����ݴ˴��⣮
��� �⣺��1����֪1molʯī��ȫת��Ϊ���ʯ��Ҫ����1.9kJ����������ʯīת��Ϊ���ʯ���Ȼ�ѧ��Ӧ����ʽΪC��ʯī���TC�����ʯ����H=+1.9kJ/mol��
�ʴ�Ϊ��C��ʯī���TC�����ʯ����H=+1.9kJ/mol��
��2��ʯī�������·�Ӧ��ʯī�����������ʾ�ת��Ϊ��Ӧ���Ȼ���������ʵĺ�����֪������I���Ȼ�����ҪΪSiCl4��AlCl3��FeCl3�ȣ�����I��̼��������ҪΪCO��SiCl4�ķе�Ϊ57.6�棬�����Ȼ���ķе������150�棬80����ȴ�õ����������SiCl4��CO����Ŀ��Ϊ��������ͷǽ���������ɻ���̿�õ������Ļ�ѧ��Ӧ����ʽΪ��2C+2Cl2+SiO2$\frac{\underline{\;����\;}}{\;}$SiCl4+2CO��
�ʴ�Ϊ����������ͷǽ��������2C+2Cl2+SiO2$\frac{\underline{\;����\;}}{\;}$SiCl4+2CO��
��3�������Ȼ���ķе������150�棬�������д���AlCl3��FeCl3��MgCl2������FeCl3��MgCl2�����������������Һ��Ӧ�õ����������Ȼ��������������������Һ��Ӧ����ƫ�����ƣ����衢���˵õ���ҺIV������ҺIV�е��������У�AlO2-��OH-��Cl-��
�ʴ�Ϊ�����ˣ�AlO2-��OH-��Cl-��
��3���������Ϸ�������������AlCl3��FeCl3��MgCl2������FeCl3��MgCl2�����������������Һ��Ӧ�õ����������Ȼ��������������������Һ��Ӧ����ƫ�����ƣ���Ӧ�����ӷ�Ӧ����ʽΪ��Al3++4OH-=AlO2-+2H2O��Fe3++3OH-=Fe��OH��3����Mg2++2OH-=Mg��OH��2�����ʴ�Ϊ��Al3++4OH-=AlO2-+2H2O��Fe3++3OH-=Fe��OH��3����Mg2++2OH-=Mg��OH��2����
��4��ƫ�����Ʒ���ˮ�⣬��������������ȥ�������������ƣ��Ҽ���������ˮ��ƽ��һֱ�����ƶ����õ��������������������ơ��Ҵ�������ҺIV���ɳ���V���ܷ�Ӧ�����ӷ���ʽΪAlO2-+CH3COOCH2CH3+2H2O $\frac{\underline{\;\;��\;\;}}{\;}$CH3COO-+CH3CH2OH+Al��OH��3����Al2O3����������Ϊ5.1%����1kg����ʯī��������������=1kg��5.1%=0.051kg������AlԪ���غ㣬��֪��������������Ϊ $\frac{0.051kg��\frac{54}{102}}{\frac{27}{78}}$=0.078kg��
�ʴ�Ϊ����������������ȥ�������������ƣ��Ҽ��������´ٽ�ƫ������ˮ��ƽ��һֱ�����ƶ����õ��������������������ơ��Ҵ�����Ӧ���ӷ���ʽΪAlO2-+CH3COOCH2CH3+2H2O $\frac{\underline{\;\;��\;\;}}{\;}$CH3COO-+CH3CH2OH+Al��OH��3����0.078��
���� ���⿼����������ᴿ���ۺ�Ӧ�ã�Ϊ��Ƶ���㣬�������ʵ����ʡ������еķ�Ӧ���������뷽��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��NH4+����c��SO42-����c��H+����c��OH-�� | B�� | c��NH4+��=2c��SO42-�� | ||
| C�� | c��NH4+��+c��NH3•H2O��=2c��SO42-�� | D�� | c��NH4+��+c��H+��=c��OH-��+2c��SO42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܣ���=�ڣ��� | B�� | �٣��ܣ��ڣ��� | C�� | �ܣ��٣��ۣ��� | D�� | �ܣ��ڣ��٣��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£���VmL0.01mol•L-1��BOH��Һ�еμ�0.01mol•L-1���ᣬ��ҺpH���������֮��Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������
�����£���VmL0.01mol•L-1��BOH��Һ�еμ�0.01mol•L-1���ᣬ��ҺpH���������֮��Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������| A�� | BOH���뷽��ʽΪBOH�TB++OH- | |
| B�� | ��������Һ��pH=2 | |
| C�� | ��c��ʾ����Һ��c��OH-��=1.0��10-6mol•L-1 | |
| D�� | BOH��aq��+HCl��aq���TBCl��aq��+H2O��l����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
 �����£���20mLijŨ�ȵ������е���0.1mol•L-1��ˮ����Һ��ˮ�������������Ũ������백ˮ������仯��ͼ��ʾ�����з�����ȷ�ǣ�������
�����£���20mLijŨ�ȵ������е���0.1mol•L-1��ˮ����Һ��ˮ�������������Ũ������백ˮ������仯��ͼ��ʾ�����з�����ȷ�ǣ�������| A�� | �������Ũ��Ϊ1mol•L-1 | |
| B�� | b����ʾ��Һ�У�c��NH4+��=2c��SO42-�� | |
| C�� | V=40 | |
| D�� | c����ʾ��Һ�У�c��H+��-c��OH-���Tc��NH3•H2O�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-��-2-�һ����� | B�� | 3-��--��ϩ | ||
| C�� | 2-��-4-��Ȳ | D�� | 1��2��4-���ױ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʹ���۵⻯����ֽ����ɫ����Һ��Na+��H+��I-��SO32- | |
| B�� | ����CO2����Һ�У�Ca2+��K+��NO3-��Cl- | |
| C�� | ��pH=14����Һ�У�Na+��K+��Cl-��SO2 | |
| D�� | ��ɫ����Һ��Na+��Ba2+��MnO4-��Cl- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com