(2012?万安县模拟)能源问题是人类社会面临的重大课题,日本大地震引起的核泄漏事故引起了人们对核能源的恐慌.而甲醇是未来重要的绿色能源之一.以CH
4和H
2O为原料,通过下列反应来制备甲醇.
①CH
4(g)+H
2O(g)=CO(g)+3H
2(g)△H=+206.0kJ/mol
②CO(g)+2H
2(g)=CH
3OH(g)△H=-129.0kJ/mol
(l)CH
4(g)与H
2O(g)反应生成CH
3OH(g)和H
2(g)的热化学方程式为
CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+77.0KJ/L
CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+77.0KJ/L
.
(2)将1.0molCH
4和2.0molH
2O(g)通过容积为100L的反应室,在一定条件下发生反应I,测得在一定的压强下CH
4的转化率与温度的关系如图1.
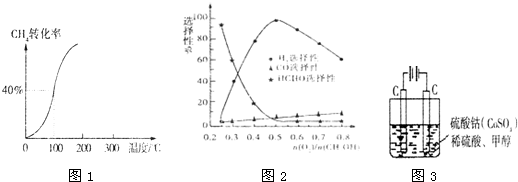
①假设100℃时达到平衡所需的时间为5min,则用H
2表示该反应的平均反应速率为
0.0024mol/L?min
0.0024mol/L?min
;
②100℃时反应I的平衡常数为
7.2×10-5(mol/L)2
7.2×10-5(mol/L)2
.
(3)在压强为0.1MPa、温度为300℃条件下,将1.0molCO与2.0molH
2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的
,其他条件不变,对平衡体系产生的影响是
CD
CD
(填字母序号).
A.c(H
2)减小 B.正反应速率加快,逆反应速率减慢
C.CH
3OH的物质的量增加 D.重新平衡时
减小 E.平衡常数K增大
(4)工业上利用甲醇制备氢气的常用方法有两种:
①甲醇蒸气重整法.该法中的一个主要反应为CH
3OH(g)?CO(g)+2H
2(g),此反应能自发进行的原因是:
反应是熵增加的反应
反应是熵增加的反应
.
②甲醇部分氧化法.在一定温度下以Ag/CeO
2-ZnO为催化剂时原料气比例对反应的选择性(选择性越大,表示生成的该物质越多)影响关系如图2所示.则当n(O
2)/n(CH
3OH)=0.25时,CH
3OH与O
2发生的主要反应方程式为
.
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co
2+氧化成Co
3+,然后以Co
3+做氧化剂把水中的甲醇氧化成CO
2而净化.实验室用图3装置模拟上述过程:
①写出阳极电极反应式
Co2+-e-=Co3+
Co2+-e-=Co3+
;
②写出除去甲醇的离子方程式
6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
6Co3++CH3OH+H2O=CO2↑+6Co2++6H+;
.