
等物质的量的Fe,Mg,Al分别与足量的物质的量浓度相同的盐酸完全反应,消耗盐酸的体积比为 ( )
A.2:3:1 B.2:2:3 C.3:2:1 D.1:3:2
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
下列化合物的俗称与化学式不对应的是
A.绿矾-FeSO4·7H2O B.芒硝-Na2SO4·10H2O
C.明矾- Al2(SO4)3·12H2O D.胆矾- CuSO4·5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
对于一个可逆反应mA+nB pC+qD,在一定温度下达到平衡,反应物浓度与生成物浓度符合下面的关系式=K,式中的K为常数。在密闭容器中将CO和水蒸气的混合气加热到800 ℃时,有下列平衡:CO(g)+H2O(g)
pC+qD,在一定温度下达到平衡,反应物浓度与生成物浓度符合下面的关系式=K,式中的K为常数。在密闭容器中将CO和水蒸气的混合气加热到800 ℃时,有下列平衡:CO(g)+H2O(g)  CO2(g)+H2(g),且K=1,若将2 mol CO和10 mol H2O(g)相互混合并加热到800 ℃,则CO的转化率约为 ( )。
CO2(g)+H2(g),且K=1,若将2 mol CO和10 mol H2O(g)相互混合并加热到800 ℃,则CO的转化率约为 ( )。
A.16.7% B.50%
C.66.7% D. 83.3%
83.3%
查看答案和解析>>
科目:高中化学 来源: 题型:
要尽量除去杂质,加入的试剂必须稍过量,最后的过量物可以使用物理或化学方法除去。现要除去NaCl中少量的CaCl2、ZnCl2、Na2SO4杂质,下列选用试剂及其使用顺序正确的是 ( )
A.Na2CO3、BaCl2、HCl B.BaCl2、Na2CO3、H2SO4
C.BaCl2、Na2CO3、HCl D.Ba(NO3)2 、Na2CO3、HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式改写成化学方程式正确的是 ( )
A.Cu2++2OH-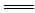 Cu(OH)2↓
Cu(OH)2↓
CuCO3+2NaOH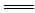 Cu(OH)2↓+Na2CO3
Cu(OH)2↓+Na2CO3
B.CO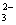 十2H+
十2H+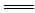 CO2↑十H2O
CO2↑十H2O
BaCO3+2HCl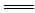 BaCl2+C02↑十H20
BaCl2+C02↑十H20
C.Ca2++CO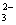
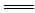 CaCO3↓
CaCO3↓
Ca(NO3)2+Na2CO3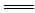 CaCO3↓+2NaNO3
CaCO3↓+2NaNO3
D.H++OH-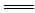 H20
H20
Ba(OH)2+H2SO4=BaSO4十2H20
查看答案和解析>>
科目:高中化学 来源: 题型:
取含MnO2的软锰矿石27.86g跟足量浓盐酸反应(杂质不参与反应),制得17.75gCl2,求
(1)这种软锰矿石中MnO2的百分含量。 (2)求被氧化的HCl的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
制备晶体硅的热方程式为 SiHCl3(l)+H2(g)=Si(s)+3HCl(g) ΔH=+238KJ/mol,
已知SiHCl3(l)=SiHCl3(g) ΔH=+10KJ/mol,相关键能数据如下表:
| SiHCl3(g) Si—H | SiHCl3(g) Si—Cl | H2(g) H—H | HCl(g) H—Cl | |
| 键能(KJ/mol) | 377 | 360 | 436 | 431 |
则晶体硅的键能为
A.186KJ/mol B.181KJ/mol C.372KJ/mol D.362KJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
下列叙述正确的是( )
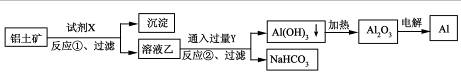
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①、过滤后所得沉淀为氢氧化铁
C.图中所示转化反应都不是氧化还原反应
D.反应②的化学方程式为NaAlO2 + CO2 + 2H2O=Al(OH)3↓ + NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年10月9日,2013年诺贝尔化学奖在瑞典揭晓,犹太裔美国理论化学家马丁·卡普拉斯、 美国斯坦福大学生物物理学家迈克尔·莱维特和南加州大学化学家亚利耶·瓦谢尔因给复杂化学体系设计了多尺度模型而分享奖项。三位科学家的研究成果已经应用于废气净化及植物的光合作用的研究中,并可用于优化汽车催化剂、药物和太阳能电池的设计。
汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) △H<0
2CO2(g)+ N2(g) △H<0
(1)同一条件下该反应正反应的平衡常数为K1,逆反应的表达式平衡常数为K2,K1与K2的关系式为 ▲ 。
(2)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 ▲ (填代号)。
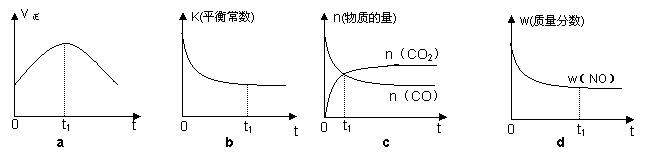

(3)在体积为10L的密闭容器中,加入一定量的CO2和H2,在900℃时发生吸热反应并记录前5min各物质的浓度,第6min改变了条件。各物质的浓度变化如下表;
| 时间/min | CO2(mol·L-1) | H2(mol·L-1) | CO(mol·L-1) | H2O(mol·L-1) |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
①前2min,用CO表示的该化学反应的速率为 ▲ ;
②第5—6min,平衡移动的可能原因是 ▲ ;
(4)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
2NO2(g)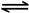 N2O4(g) △H=-56.9 kJ·mol-1
N2O4(g) △H=-56.9 kJ·mol-1
H2O(g) = H2O(l) △H = -44.0 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
▲ 。
(5)在一定条件下,可以用NH3处理NOx。已知NO与NH3发生反应生成N2和H2O,现有NO和NH3的混合物1mol,充分反应后得到的还原产物比氧化产物多1.4 g,则原反应混合物中NO的物质的量可能是 ▲ mol
(6)在一定条件下,也可以用H2处理CO合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者以物质的量11催化反应,其原子利用率达100%,合成的物质可能是 ▲ 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com