
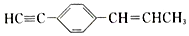
 的说法中不正确的是( )
的说法中不正确的是( )| A. | 最多只有5个碳原子在同一直线上 | B. | 最多有11个碳原子在同一平面上 | ||
| C. | 有7个碳原子可能在同一直线上 | D. | 最多有19个原子在同一平面上 |
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:推断题
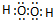 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn与稀硫酸反应制取H2时,加入少量硫酸铜 | |
| B. | Al和稀硫酸反应制取H2时,将稀硫酸换成浓硫酸 | |
| C. | 石灰石与稀盐酸反应生成CO2时,将石灰石粉碎 | |
| D. | 用KClO3固体分解制取O2时,固体中添加少量MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A. | 该反应的正反应是吸热反应 | |
| B. | 该反应达到平衡后,保持容器体积不变升高温度,正反应速率不变,容器内混合气体的压强不变 | |
| C. | 830℃时,在恒容反应器中按物质的量比n(CO):n(H2O):n(H2):n(CO2)=2:4:6:1投入反应混合物发生上述反应,初始时刻υ正<υ逆 | |
| D. | 830℃时,在2 L的密闭容器中加入4 mol CO(g)和6 mol H2O(g)达到平衡时,CO的转化率是60% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
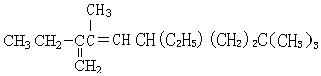 3,8,8-三甲基-2,5-二乙基-1,3-壬二烯
3,8,8-三甲基-2,5-二乙基-1,3-壬二烯 6-甲基-6-乙基-2-辛炔.
6-甲基-6-乙基-2-辛炔.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
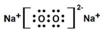
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
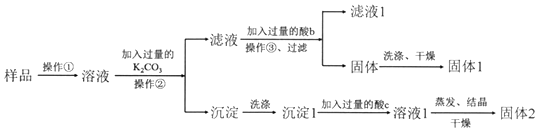
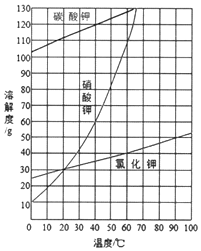
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com