
 µŚĖÄÖÜĘŚ¹ż¶ÉŌŖĖŲFe”¢TiæÉÓėC”¢H”¢N”¢OŠĪ³É¶ąÖÖ»ÆŗĻĪļ£®
µŚĖÄÖÜĘŚ¹ż¶ÉŌŖĖŲFe”¢TiæÉÓėC”¢H”¢N”¢OŠĪ³É¶ąÖÖ»ÆŗĻĪļ£®·ÖĪö £Ø1£©¢ŁĶ¬ÖÜĘŚŌŖĖŲ“Ó×óµ½ÓŅŌŖĖŲµÄµēøŗŠŌÖš½„Ōö“󣬷Ē½šŹōŠŌŌ½ĒæµēøŗŠŌŌ½“ó£»
¢ŚA£®¼×Č©ŗĶĖ®·Ö×Ó¼äÄÜŠĪ³ÉĒā¼ü£»
B£®CO2ŹĒÖ±ĻߊĶ½į¹¹£¬Ģ¼Ō×ÓŹĒspŌӻƣ»
C£®±½·Ö×ÓÖŠµÄĢ¼Ģ¼¼ü¼Č²»ŹĒĢ¼Ģ¼µ„¼ü£¬Ņ²²»ŹĒĢ¼Ģ¼Ė«¼ü£¬¶ųŹĒŅ»ÖÖ½éÓŚĢ¼Ģ¼µ„¼üŗĶĢ¼Ģ¼Ė«¼üÖ®¼äµÄ¶ĄĢŲµÄ¼ü£¬»¹ÓŠ6øöC-H¦Ņ¼ü£»
D£®CO2ŹĒ·Ö×Ó¾§Ģ壬¶žŃõ»Æ¹čŹĒŌ×Ó¾§Ģ壻
¢Ūøł¾ŻŌ×Ó×īĶā²ćµē×ÓŹżČ·¶ØŌ×ÓŠĪ³ÉµÄ¹²¼Ū¼üŹżÄ棻
£Ø2£©¢ŁÅäĢåÖŠ±ŲŠčŗ¬ÓŠ¹Ā¶Ōµē×Ó£¬·ńŌņ²»ÄÜŠĪ³ÉÅäĪ»¼ü£»
¢ŚĮłĒčŗĻŃĒĢśĄė×Ó[Fe£ØCN£©6]4-ÖŠFe2+ÓėCN-ŠĪ³ÉÅäĪ»¼ü£¬CN-ÖŠ“ęŌŚC”ŌNČż¼ü£¬ĪŖ¼«ŠŌ¹²¼Ū¼ü£¬Čż¼üÖŠÓŠ1øö¦Ņ¼ü2øö¦Š¼ü£»
µē×ÓŹżŗĶŌ×ÓŹż·Ö±š¶¼ĻąµČµÄĪ¢Į£»„ĪŖµČµē×ÓĢ壮
£Ø3£©ĒųµÄĆū³ĘĄ“×ŌÓŚ°“¹¹ŌģŌĄķ×īŗóĢīČėµē×ÓµÄÄܼ¶Ćū³Ę£¬ĖłŅŌøł¾Ż¹¹ŌģŌĄķæÉÖŖTiŹōÓŚdĒų£»
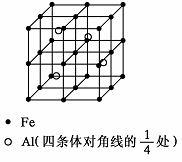
£Ø4£©øł¾Ż¾§°ūµÄ½į¹¹æÉÖŖ£¬ŗ¬ÓŠµÄĢśŌ×ÓŹĒ8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$+12”Į$\frac{1}{4}$+1=8£®ĀĮŌŚ¾§°ūÄŚ²æ£¬ĖłŅŌŗ¬ÓŠ4øöĀĮŌ×Ó£¬Ņņ“Ė»ÆѧŹ½ĪŖFe2Al£®±ķŹ¾³ö¾§°ūÖŹĮ棬Éč“ĖŗĻ½šÖŠ×ī½üµÄĮ½øöFeŌ×ÓÖ®¼äµÄ¾ąĄėĪŖx£¬Ōņ¾§°ūĄā³¤ĪŖ2x£¬øł¾Żm=¦ŃV¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©¢ŁĶ¬ÖÜĘŚŌŖĖŲ“Ó×óµ½ÓŅŌŖĖŲµÄµēøŗŠŌÖš½„Ōö“󣬷Ē½šŹōŠŌŌ½ĒæµēøŗŠŌŌ½“󣬹ŹµēøŗŠŌ£ŗH£¼C£¼N£¼O£¬
¹Ź“š°øĪŖ£ŗH£¼C£¼N£¼O£»
¢Śa£®ŃõŌŖĖŲµēøŗŠŌŗÜĒ棬¼×Č©ÖŠŃõŌŖĖŲÓėĖ®æÉŅŌŠĪ³ÉĒā¼ü£¬¹ŹaÕżČ·£»
b£®HCHO·Ö×ÓÖŠCŌ×Ó²ÉÓĆsp2Ōӻƣ¬µ«¶žŃõ»ÆĢ¼·Ö×ÓÖŠCŌ×ÓĪŖspŌӻƣ¬¹Źb“ķĪó£»
c£®C2H2ŹĒÖ±ĻߊĶ¶Ō³Ę½į¹¹£¬ĪŖ·Ē¼«ŠŌ·Ö×Ó£¬µ«±½ÖŠĢ¼Ģ¼¼üŗ¬ÓŠ6øö¦Ņ¼ü£¬ĆæøöĢ¼Ēā¼üŗ¬ÓŠŅ»øö¦Ņ¼ü£¬±½·Ö×ÓÖŠŅ»¹²ŗ¬ÓŠ12øö£¬¹Źc“ķĪó£»
d£®¶žŃõ»ÆĢ¼¾§ĢåŹĒ·Ö×Ó¾§Ģ壬¶žŃõ»Æ¹č¾§ĢåŹĒŌ×Ó¾§Ģ壬ĖłŅŌCO2¾§ĢåµÄČŪµć”¢·Šµć¶¼±Č¶žŃõ»Æ¹č¾§ĢåµÄµĶ£¬¹ŹdÕżČ·£¬
¹Ź“š°øĪŖ£ŗbc£»
¢ŪĒčĖį£ØHOCN£©ŹĒŅ»ÖÖĮ“ד·Ö×Ó£¬ĒŅĘä·Ö×ÓÄŚø÷Ō×Ó×īĶā²ć¾łŅŃ“ļµ½ĪČ¶Ø½į¹¹£¬Ģ¼³É4øö¹²¼Ū¼ü£¬µŖ³É3øö¹²¼Ū¼ü£¬Ńõ³É2øö¹²¼Ū¼ü£¬H³É1øö¹²¼Ū¼ü£¬¹ŹĘä½į¹¹¼ņŹ½ĪŖN”ŌC-O-H£¬
¹Ź“š°øĪŖ£ŗN”ŌC-O-H£»
£Ø2£©¢ŁÓėFeŌ×Ó»ņĄė×ÓŠĪ³ÉÅäŗĻĪļµÄ·Ö×Ó»ņĄė×ÓĪŖÅäĢ壬Ӧ¾ß±øµÄ½į¹¹ĢŲÕ÷ŹĒ£ŗ¾ßÓŠ¹Ā¶Ōµē×Ó¶Ō£¬¹Ź“š°øĪŖ£ŗ¾ßÓŠ¹Ā¶Ōµē×Ó£»
¢ŚĮłĒčŗĻŃĒĢśĄė×Ó[Fe£ØCN£©6]4-ÖŠFe2+ÓėCN-ŠĪ³ÉÅäĪ»¼ü£¬CN-ÖŠ“ęŌŚC”ŌNČż¼ü£¬ĪŖ¼«ŠŌ¹²¼Ū¼ü£¬Čż¼üÖŠÓŠ1øö¦Ņ¼ü2øö¦Š¼ü£¬ĖłŅŌCN-ÖŠ¹²¼Ū¼ü”¢ÅäĪ»¼ü”¢¦Ņ¼ü”¢¦Š¼ü£¬·Ö×ÓÖŠ²»“ęŌŚ·Ē¼«ŠŌ¼ü£¬
CN-ÖŠCŌ×ÓÓė1øöµ„Ī»øŗµēŗÉÓĆNŌ×ÓĢę»»æɵĆCN-µČµē×ÓĢåµÄµ„ÖŹĪŖN2£¬
¹Ź“š°øĪŖ£ŗB£»N2£»
£Ø3£©TiŌ×ÓŗĖĶāµē×ÓÅŲ¼ĪŖ1s22s22p63s23p63d24s2£¬īŃĪ»ÓŚµŚĖÄÖÜĘŚµŚ¢ōB×壬µē×Ó×īŗóĢī³äd¹ģµĄ£¬ŹōÓŚdĒųŌŖĖŲ£¬¹Ź“š°øĪŖ£ŗd£»
£Ø4£©¢Łøł¾Ż¾§°ūµÄ½į¹¹æÉÖŖ£¬ŗ¬ÓŠµÄĢśŌ×ÓŹĒ8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$+12”Į$\frac{1}{4}$+1=8£®ĀĮŌŚ¾§°ūÄŚ²æ£¬ĖłŅŌŗ¬ÓŠ4øöĀĮŌ×Ó£¬Ņņ“Ė»ÆѧŹ½ĪŖFe2Al£¬¹Ź“š°øĪŖ£ŗFe2Al£»
¢Ś¾§°ūÖŹĮæĪŖ$\frac{4”Į139}{{N}_{A}}$g£¬Éč“ĖŗĻ½šÖŠ×ī½üµÄĮ½øöFeŌ×ÓÖ®¼äµÄ¾ąĄėĪŖx£¬Ōņ¾§°ūĄā³¤ĪŖ2x£¬Ōņ$\frac{4”Į139}{{N}_{A}}$g=£Ø2x£©3”Į¦Ńg/cm3£¬½āµĆx=$\root{3}{{\frac{139}{{2{N_A}¦Ń}}}}$cm£¬¹Ź“š°øĪŖ£ŗ$\root{3}{{\frac{139}{{2{N_A}¦Ń}}}}$£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹ½į¹¹ŗĶŠŌÖŹ£¬ĢāÄæ±Č½Ļ×ŪŗĻ£¬²ąÖŲ¶ŌĪļÖŹ½į¹¹Ö÷øÉÖŖŹ¶µÄ漲飬Éę¼°µēøŗŠŌ”¢ŌÓ»ÆĄķĀŪ”¢»Æѧ¼ü”¢·Ö×Ó½į¹¹ÓėŠŌÖŹ”¢¾§ĢåĄąŠĶÓėŠŌÖŹ”¢¾§°ū¼ĘĖćµČ£¬ŠčŅŖѧɜ¾ß±øÖŖŹ¶µÄ»ł“”£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
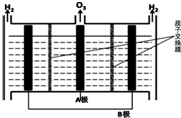 NOÄÜŅżĘš¹ā»ÆѧŃĢĪķ£¬ĘĘ»µ³ōŃõ²ć£®“¦ĄķNOÓŠ¶ąÖÖ·½·Ø£¬øł¾ŻĢāŅā»Ų“šĻĀĮŠĪŹĢā£ŗ
NOÄÜŅżĘš¹ā»ÆѧŃĢĪķ£¬ĘĘ»µ³ōŃõ²ć£®“¦ĄķNOÓŠ¶ąÖÖ·½·Ø£¬øł¾ŻĢāŅā»Ų“šĻĀĮŠĪŹĢā£ŗ| Ź±¼ä£Øs£© | 0 | 1 | 2 | 3 | 4 | ” |
| c£ØNO£©/mol•L-1 | 1.00”Į10-3 | 4.00”Į10-4 | 1.70”Į10-4 | 1.00”Į10-4 | 1.00”Į10-4 | ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅ“¼Ź¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬ŹĒŅņĪŖ·¢ÉśĮĖŃõ»Æ·“Ó¦ | |
| B£® | ½«±½¼ÓČėäåĖ®ÖŠ£¬Õńµ“ŗóĖ®²ć½Ó½üĪŽÉ«£¬ŹĒŅņĪŖ·¢ÉśĮĖČ”“ś·“Ó¦ | |
| C£® | ŅŅĻ©Ź¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«£¬ŹĒŅņĪŖ·¢ÉśĮĖ¼Ó³É·“Ó¦ | |
| D£® | ¼×ĶéÓėĀČĘų»ģŗĻ£¬¹āÕÕŅ»¶ĪŹ±¼äŗó»ĘĀĢÉ«ĻūŹ§£¬ŹĒŅņĪŖ·¢ÉśĮĖČ”“ś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

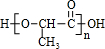 £®
£®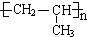 £¬øĆ·“Ó¦ĄąŠĶŹĒ¼Ó¾Ū·“Ó¦£®
£¬øĆ·“Ó¦ĄąŠĶŹĒ¼Ó¾Ū·“Ó¦£®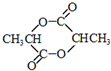 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

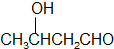 $”ś_{¢Ś}^{”÷}$CH3CH=CHCHO
$”ś_{¢Ś}^{”÷}$CH3CH=CHCHO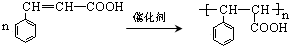 £®
£®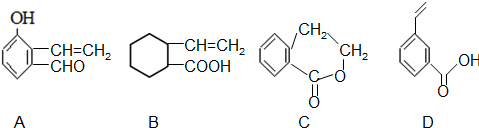
 ”śE µÄŗĻ³ÉĀ·Ļß£ØŹŌ¼Į¼°ČܼĮČĪŃ”£ŗŗĻ³ÉĀ·Ļß²ĪÕÕ”°ŅŃÖŖ¢Ł”±ÖŠŹéŠ“ŠĪŹ½£©
”śE µÄŗĻ³ÉĀ·Ļß£ØŹŌ¼Į¼°ČܼĮČĪŃ”£ŗŗĻ³ÉĀ·Ļß²ĪÕÕ”°ŅŃÖŖ¢Ł”±ÖŠŹéŠ“ŠĪŹ½£© £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
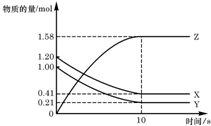 Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚ 2L µÄĆܱÕČŻĘ÷ÖŠ£¬X”¢Y”¢Z ČżÖÖĘųĢåµÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĆčŹöÕżČ·µÄŹĒ£Ø””””£©
Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚ 2L µÄĆܱÕČŻĘ÷ÖŠ£¬X”¢Y”¢Z ČżÖÖĘųĢåµÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĆčŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | ·“Ó¦æŖŹ¼µ½ 10s£¬ÓĆ Z ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ 0.158mol/£ØL•s£© | |
| B£® | ·“Ó¦æŖŹ¼µ½ 10s£¬X µÄĪļÖŹµÄĮæÅØ¶Č¼õÉŁĮĖ 0.79mol/L | |
| C£® | ·“Ó¦æŖŹ¼µ½ 10s£¬Y µÄ×Ŗ»ÆĀŹĪŖ 79.0% | |
| D£® | ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗX£Øg£©+Y£Øg£©?Z£Øg£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃéŹĀŹµ | ĄķĀŪ½āŹĶ |
| A | µŖŌ×ӵĵŚŅ»µēĄėÄÜ“óÓŚŃõŌ×Ó | µŖŌ×Ó2pÄܼ¶°ė³äĀś |
| B | CO2µÄČŪµćøßÓŚCH4 | Ģ¼Ńõ¼ü¼üÄÜ“óÓŚĢ¼Ēā¼ü |
| C | H2OµÄ·ŠµćøßÓŚH2S | H2O·Ö×Ó¼äŠĪ³ÉĮĖĒā¼ü |
| D | ½šøÕŹÆµÄÓ²¶Č“óÓŚ¾§Ģå¹č | Ģ¼Ģ¼¼ü¼üÄÜ“óÓŚ¹č¹č¼ü |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com