
| 容器编号 | 起始时各物质 物质的量/mol | 平衡时反应中的能量变化 | ||
| NH3 | N2 | H2 | ||
| ① | 2 | 0 | 0 | 吸收热量a kJ |
| ② | 0 | 1 | 3 | 放出热量b kJ |
| ③ | 4 | 0 | 0 | 吸收热量c kJ |
| A、热量关系:a=b |
| B、①②③反应的平衡常数:③>①>② |
| C、达平衡时H2的体积分数:①>③ |
| D、①中的密度不再改变时说明反应已达到平衡状态 |
| C 2(NH 3) |
| C(N 2).C 3(H2) |
| C(N 2).C 3(H 2) |
| C 2(NH 3) |
| C 2(NH 3) |
| C(N 2).C 3(H2) |
| C(N 2).C 3(H 2) |
| C 2(NH 3) |


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
| A、室温下,向0.01 mol/L NHHSO溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| B、0.1 mol/L NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+) |
| C、Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) |
| D、25℃时,浓度均为0.1 mol/L的CH3COOH、CH3COONa混合溶液的pH=4.75:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 3 |
| 2 |
| 3 |
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,金属钠可以成为绝缘体 |
| B、一定条件下,水在20℃时能凝固成固体 |
| C、用斧头将木块一劈为二,在这个过程中个别原子恰好分成更小微粒 |
| D、几千万年前地球上一条恐龙体内的某个原子可能在你的身体里 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①②⑤⑥ |
| C、③⑤⑥⑦ | D、①③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
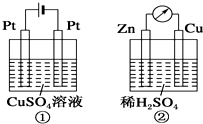 如图所示的两个装置中,溶液的体积 均为200mL,开始时电解质溶液的浓度均为0.1mol/L.工作一段时间后,测得导线中均通过0.02mol电子.若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个装置中,溶液的体积 均为200mL,开始时电解质溶液的浓度均为0.1mol/L.工作一段时间后,测得导线中均通过0.02mol电子.若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )| A、产生气体的体积:①>② |
| B、溶液的pH变化:①增大,②减小 |
| C、电极上析出固体物质的质量:①>② |
| D、电极反应式:①的阴极:Cu2++2e-═Cu,②的负极:2H++2e-═H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com