
·ÖĪö £Ø1£©·“Ó¦3S8+48NaH=16Na2S+8Na2SO3+24H2OÖŠSµÄ»ÆŗĻ¼Ū“Ó0¼ŪÉżøßµ½+4¼Ū£¬½µµĶµ½-2¼Ū£¬HŌŖĖŲµÄ»ÆŗĻ¼Ū“Ó-1¼ŪÉżøßµ½+1¼Ū£¬¾Ż“Ė·ÖĪö£»
£Ø2£©·“Ó¦2Na2S2O3+I2=2NaI+Na2S4O6ÖŠIµÄ»ÆŗĻ¼Ū“Ó0¼Ū½µµĶµ½-1¼Ū£¬¾Ż“Ė¼ĘĖć£»
£Ø3£©·¢Éś·“Ó¦£ŗ5S2O82-+2Mn2++8H2O=2R+10SO42-+16H+£¬øł¾ŻŌŖĖŲŹŲŗćæÉÖŖ£¬RÖŠŗ¬ÓŠMnŗĶOŌŖĖŲ£®
½ā“š ½ā£ŗ£Ø1£©·“Ó¦3S8+48NaH=16Na2S+8Na2SO3+24H2OÖŠSµÄ»ÆŗĻ¼Ū“Ó0¼ŪÉżøßµ½+4¼Ū£¬½µµĶµ½-2¼Ū£¬ĖłŅŌHŌŖĖŲµÄ»ÆŗĻ¼Ū“Ó-1¼ŪÉżøßµ½+1¼Ū£¬Ńõ»Æ¼ĮĪŖS8£»
Ńõ»Æ²śĪļĪŖNa2SO3ŗĶH2O£¬»¹Ō²śĪļĪŖNa2S£¬ŌņŃõ»Æ²śĪļÓė»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČĪŖ£Ø8+24£©£ŗ16=2£ŗ1£»
¹Ź“š°øĪŖ£ŗS8£»2£ŗ1£»
£Ø2£©·“Ó¦2Na2S2O3+I2=2NaI+Na2S4O6ÖŠIµÄ»ÆŗĻ¼Ū“Ó0¼Ū½µµĶµ½-1¼Ū£¬Ōņ1mol I2²ĪÓė·“Ó¦×ŖŅʵē×ÓŹżÄæĪŖ2NAøö£»
¹Ź“š°øĪŖ£ŗ2NA£»
£Ø3£©·¢Éś·“Ó¦£ŗ5S2O82-+2Mn2++8H2O=2R+10SO42-+16H+£¬ŌŖĖŲŹŲŗćæÉÖŖ£¬RÖŠŗ¬ÓŠMnŗĶOŌŖĖŲ£¬ÓɵēŗÉŹŲŗćæÉÖŖ£¬Rŗ¬ÓŠŅ»øöøŗµēŗÉ£¬ŌņRĪŖMnO4-£»
¹Ź“š°øĪŖ£ŗB£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»Æ»¹Ō·“Ó¦µÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬Éę¼°Ńõ»Æ»¹Ō·“Ó¦µÄÅäĘ½”¢¼ĘĖć£¬Ć÷Č·Ńõ»Æ»¹Ō·“Ó¦µÄŹµÖŹĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
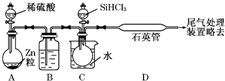 ¾§Ģå¹čŹĒŅ»ÖÖÖŲŅŖµÄ·Ē½šŹō²ÄĮĻ£¬Öʱø“æ¹čµÄÖ÷ŅŖ²½ÖčČēĻĀ£ŗ
¾§Ģå¹čŹĒŅ»ÖÖÖŲŅŖµÄ·Ē½šŹō²ÄĮĻ£¬Öʱø“æ¹čµÄÖ÷ŅŖ²½ÖčČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2NO2£Øg£©?N2O4£Øg£© | B£® | 2HI£Øg£©?H2£Øg£©+I2£Øg£© | ||
| C£® | PCl5?PCl3£Øg£©+Cl2£Øg£© | D£® | CaCO3£Øs£©?CaO£Øg£©+CO2 £Øg£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
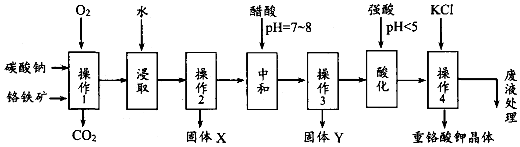
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ś¢Ū | C£® | ¢Ł¢Ü¢Ż | D£® | ¢Ł¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
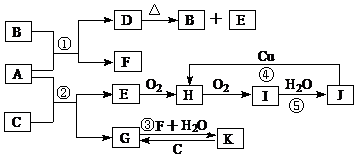
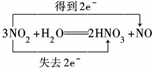 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ3 | B£® | 2£ŗ3 | C£® | 1£ŗ4 | D£® | 2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆ·“Ó¦ŹĒÖĆ»»·“Ó¦ | B£® | øĆ·“Ó¦ÖŠFeCl3×÷»¹Ō¼Į | ||
| C£® | »¹ŌŠŌ£ŗFe£¾Cu | D£® | Ńõ»ÆŠŌ£ŗCuCl2£¾FeCl3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
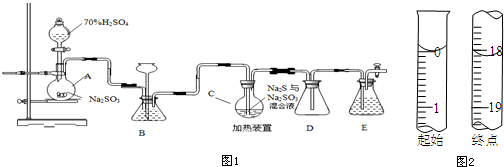
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com