
¶ĢÖÜĘŚŌŖĖŲA”¢B”¢CµÄŌ×ÓŠņŹżÖ®ŗĶĪŖ37£¬A”¢BŌŚĶ¬Ņ»ÖÜĘŚ£¬A+”¢C-¾ßÓŠĻąĶ¬µÄŗĖĶāµē×Ó²ć½į¹¹”£ĻĀĮŠĶĘ²ā²»ÕżČ·µÄŹĒ( )
A. Ķ¬ÖÜĘŚŌŖĖŲÖŠCµÄĒā»ÆĪļĪČ¶ØŠŌ×īĒæ
B. Ķ¬ÖÜĘŚŌŖĖŲÖŠAµÄ½šŹōŠŌ×īĒæ
C. Ō×Ó°ė¾¶£ŗA>B£¬Ąė×Ó°ė¾¶£ŗA+>C-
D. A”¢B”¢CµÄ¼ņµ„Ąė×ÓÖŠ£¬»įĘĘ»µĖ®µÄµēĄėĘ½ŗāµÄŹĒC

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģÄŚĆɹÅøßČżÉĻ9ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éĪļÖŹĻą»„»ģŗĻ·“Ó¦ŗó£¬×īÖÕÓŠ°×É«³ĮµķÉś³ÉµÄŹĒ£Ø £©
¢ŁÉŁĮæCa( OH)2Ķ¶Čė¹żĮæNaHCO3ČÜŅŗÖŠ
OH)2Ķ¶Čė¹żĮæNaHCO3ČÜŅŗÖŠ
¢Ś¹żĮæNaOHČÜŅŗŗĶĆ÷·ÆČÜŅŗ»ģŗĻ
¢Ū½šŹōÄĘĶ¶Čėµ½FeCl2ÖŠ
¢ÜĻņNaAlO2ČÜŅŗÖŠĶØČė¹żĮæCO2[
¢ŻĻņ±„ŗĶNa2CO3ČÜŅŗÖŠĶØČė¹żĮæCO2
A£®¢Ł¢Ś¢Ū¢Ü¢Ż B£®Ö»ÓŠ¢Ł¢Ü¢Ż C£®Ö»ÓŠ¢Ś¢Ū D£®Ö»ÓŠ¢Ū¢Ü
D£®Ö»ÓŠ¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½Ī÷Ź”øßČżÉĻѧʌµŚ¶ž“Ī¶Īæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆѧŌŚ¹¤Å©ŅµÉś²śŗĶČÕ³£Éś»īÖŠ¶¼ÓŠ×ÅÖŲŅŖµÄÓ¦ÓĆ”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ( )
A£®ĄūÓĆ“ß»ÆÉ菩£¬æÉŅŌ½«Ęū³µĪ²ĘųÖŠCOŗĶNO×Ŗ»ÆĪŖĪŽŗ¦ĘųĢå
B£®°ėµ¼Ģ劊ŅµÖŠÓŠŅ»¾ä»°£ŗ”°“ÓɳĢ²µ½ÓĆ»§”±£¬¼ĘĖ滜Š¾Ę¬µÄ²ÄĮĻŹĒ¶žŃõ»Æ¹č
C£®¹ųĀÆĖ®¹øÖŠŗ¬ÓŠ µÄCaSO4£¬æÉĻČÓĆNa2CO3ČÜŅŗ“¦Ąķ£¬ŗóÓĆĖį³żČ„
µÄCaSO4£¬æÉĻČÓĆNa2CO3ČÜŅŗ“¦Ąķ£¬ŗóÓĆĖį³żČ„
D£®·ĄÖ¹ĖįÓź·¢ÉśµÄÖŲŅŖ“ėŹ©Ö®Ņ»ŹĒŹ¹ÓĆĒå½ąÄÜŌ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½ĖÕŹ”ĪŽĪżŹŠČżŠ£ĮŖŗĻĢåøßČżÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
“Óŗ£“ųÖŠÖĘČ”µ„ÖŹµāŠčŅŖ¾¹ż×ĘÉÕ”¢Čܽā”¢¹żĀĖ”¢Ńõ»Æ”¢ŻĶČ””¢·ÖŅŗ”¢ÕōĮóµČ²Ł×÷”£ĻĀĮŠĶ¼Ź¾¶ŌÓ¦µÄ×°ÖĆŗĻĄķ”¢²Ł×÷¹ę·¶µÄŹĒ

A£®×ĘÉÕ B£®¹żĀĖ C£®·ÖŅŗ D£®ÕōĮó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗžÄĻŹ”ŅęŃōŹŠøßČżÉĻѧʌµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŠæŹĒŅ»ÖÖ³£ÓĆ½šŹō£¬ļŲ£ØGa£©µÄ»ÆŗĻĪļµŖ»ÆļŲ£ØGaN£©ŹĒÖĘŌģLEDµÄÖŲŅŖ²ÄĮĻ£¬±»ÓžĪŖµŚČż“ś°ėµ¼Ģå²ÄĮĻ”£
I£®ļŲ£ØGa£©ŹĒ»š·ØŅ±Į¶Šæ¹ż³ĢÖŠµÄø±²śĘ·£¬ļŲÓėĀĮĶ¬Ö÷×åĒŅĻąĮŚ£¬»ÆѧŠŌÖŹÓėĀĮĻąĖĘ”£
¢ÅGaµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ ___________________”£
¢ĘGaNæÉÓÉGaŗĶNH3ŌŚøßĪĀĢõ¼žĻĀÖĘČ”£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
¢ĒĻĀĮŠÓŠ¹ŲļŲŗĶļŲµÄ»ÆŗĻĪļµÄĖµ·ØÕżČ·µÄŹĒ____ ”£
A£®³£ĪĀĻĀ£¬GaæÉÓėĖ®¾ēĮŅ·“Ó¦·Å³öĒāĘų
B£®Ņ»¶ØĢõ¼žĻĀ£¬GaæÉČÜÓŚŃĪĖįŗĶĒāŃõ»ÆÄĘ
C£®Ņ»¶ØĢõ¼žĻĀ£¬Ga2O3æÉÓėNaOH·“Ӧɜ³ÉŃĪ
D£®Ga2O3æÉÓÉGa(OH)3ŹÜČČ·Ö½āµĆµ½
II£®ŠæµÄŅ±Į¶·½·ØÓŠ»š·ØŗĶŹŖ·Ø”£¹¤ŅµÉĻĄūÓĆŠæ±ŗÉ°£ØÖ÷ŅŖŗ¬ZnO”¢ZnFe2O4£¬»¹ŗ¬ÓŠÉŁĮæCaO”¢FeO”¢CuO”¢NiOµČŃõ»ÆĪļ£©ŹŖ·ØÖĘČ”½šŹōŠæµÄĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ
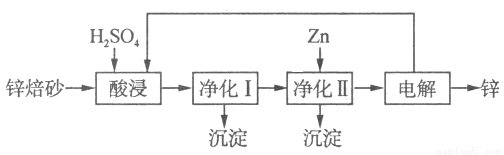
ŅŃÖŖ£ŗFeµÄ»īĘĆŠŌĒæÓŚNi
¢ČZnFe2O4æÉŅŌŠ“³ÉZnO”¤Fe2O3£¬ZnFe2O4ÓėH2SO4·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
¢É¾»»ÆI²Ł×÷·ÖĪŖĮ½²½£ŗµŚŅ»²½ŹĒ½«ČÜŅŗÖŠÉŁĮæµÄFe2+Ńõ»Æ£»µŚ¶ž²½ŹĒæŲÖĘČÜŅŗpH£¬Ö»Ź¹Fe3+×Ŗ»ÆĪŖFe(OH)3³Įµķ”£¾»»ÆIÉś³ÉµÄ³ĮµķÖŠ»¹ŗ¬ÓŠČÜŅŗÖŠµÄŠüø”ŌÓÖŹ£¬ČÜŅŗÖŠµÄŠüø”ŌÓÖŹ±»¹²Ķ¬³ĮµķµÄŌŅņŹĒ____________________”£
¢Ź¾»»ÆIIÖŠ¼ÓČėZnµÄÄæµÄŹĒ___________________”£
¢Ė³£ĪĀĻĀ£¬¾»»ÆIÖŠ£¬Čē¹ūŅŖŹ¹c(Fe3+) < 10-5 mol/L£¬ŌņÓ¦æŲÖĘČÜŅŗpHµÄ·¶Ī§ĪŖ_____________”£ŅŃÖŖ£ŗKsp[Fe(OH)3] = 8.0 ”Į 10-38£»lg5 = 0.7
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗžÄĻŹ”ŅęŃōŹŠøßČżÉĻѧʌµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃéÄÜ“ļµ½Ō¤ĘŚÄæµÄµÄŹĒ( )
±ąŗÅ | ŹµŃéÄŚČŻ | ŹµŃéÄæµÄ |
A | ŹŅĪĀĻĀ£¬ÓĆpHŹŌÖ½·Ö±š²ā¶ØÅضČĪŖ18mol/LŗĶ0.1 mol”¤L”Ŗ1H2SO4ČÜŅŗµÄpH | ±Č½Ļ²»Ķ¬ÅضČH2SO4µÄĖįŠŌĒæČõ |
B | Ļņŗ¬ÓŠ·ÓĢŖµÄNa2CO3ČÜŅŗÖŠ¼ÓČėÉŁĮæBaC12¹ĢĢ壬ČÜŅŗŗģÉ«±äĒ³ | Ö¤Ć÷Na2CO3ČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā |
C | Ļņ10mL 0.2 mol”¤L”Ŗ1 NaOHČÜŅŗÖŠµĪČė2µĪ0.1 mol”¤L”Ŗ1MgCl2ČÜŅŗ£¬²śÉś°×É«³Įµķŗó£¬ŌŁµĪ¼Ó2µĪ0.1 mol”¤L”Ŗ1FeCl3ČÜŅŗ£¬ÓÖÉś³ÉŗģŗÖÉ«³Įµķ | Ö¤Ć÷ŌŚĻąĶ¬ĪĀ¶ČĻĀµÄ Ksp[Mg(OH)2]£¾Ksp[Fe(OH)3] |
D | ÅäÖĘFeCl2ČÜŅŗŹ±£¬ĻČ½«FeCl2ČÜÓŚŹŹĮæÅØŃĪĖįÖŠ£¬ŌŁÓĆÕōĮóĖ®Ļ”ŹĶµ½ĖłŠčÅØ¶Č£¬×īŗóŌŚŹŌ¼ĮĘæÖŠ¼ÓČėÉŁĮæĶ·Ū | ŅÖÖĘFe2£«Ė®½ā£¬²¢·ĄÖ¹Fe2£«±»Ńõ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģĖÄ“ØŹ”Š£øßČżÉĻѧʌµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
”¾»Æѧ-Ń”ŠŽ3£ŗĪļÖŹ½į¹¹ÓėŠŌÖŹ”æ
A”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£AŹĒŌ×Ó°ė¼Ū×īŠ”µÄŌŖĖŲ£»BµÄ×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄ2±¶£»DµÄLÄܲćÓŠĮ½¶Ō³É¶Ōµē×Ó£»E£«µÄŗĖĶāÓŠČżøöÄÜ²ć£¬ĒŅ¶¼ĶāÓŚČ«Āś×“Ģ¬”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©»łĢ¬DŌ×ÓŗĖĶāµē×ÓµÄÅŲ¼Ź½ĪŖ___________________”£
£Ø2£©B”¢C”¢DČżÖÖŌŖĖŲµÄµēøŗŠŌÓɓ󵽊”µÄĖ³ŠņŹĒ_______________________£ØĢīŌŖĖŲ·ūŗÅ£©”£
£Ø3£©E(NH3)2+ 4Ąė×ÓµÄŃÕÉ«ŹĒ___________£»ŗ¬ÓŠ»Æѧ¼üĄąŠĶŹĒ_________________£»Ąė×ÓÖŠNŌ×ÓŌӻƹģµĄĄąŠĶŹĒ_________________”£
£Ø4£©D”¢EÄÜŠĪ³ÉĮ½ÖÖ¾§Ģ壬Ę侧°ū·Ö±šČē¼×”¢ŅŅĮ½Ķ¼”£¾§ĢåŅŅÖŠ£¬EµÄÅäĪ»ŹżĪŖ_________£»ŌŚŅ»¶ØĢõ¼žĻĀ£¬¼×ŗĶC2A4·“Ӧɜ³ÉŅŅ£¬Ķ¬Ź±Éś³ÉŌŚ³£ĪĀĻĀ·Ö±šĪŖĘųĢåŗĶŅŗĢåµÄĮķĶāĮ½ÖÖ³£¼ūĪŽĪŪČ¾ĪļÖŹ”£øĆ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ___________________________”£

£Ø5£©Čō¼×µÄĆܶČĪŖ¦Ń g/cm3£¬NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬Ōņ¼×¾§°ūµÄ±ß³¤æɱķŹ¾ĪŖ_________cm”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗžÄĻŹ”ŹµŃé°ąøßČżÉĻµŚŅ»“ĪÖŹ¼ģ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĶßĖ¹±¬ÕØŹĒĆŗæóæŖ²ÉÖŠµÄÖŲ“óĪ£ŗ¦,Ņ»ÖÖĶßĖ¹·ÖĪöŅĒ(ČēĶ¼¼×)ŌŚĆŗæóĻļµĄÖŠµÄ¼×ĶéÅØ¶Č“ļµ½Ņ»¶ØÖµŹ±,Ęä“«øŠĘ÷¾ĶæÉŅŌĻŌŹ¾”£øĆĶßĖ¹·ÖĪöŅĒ¹¤×÷ŌĄķĄąĖĘČ¼ĮĻµē³ŲµÄ¹¤×÷ŌĄķ,Ęä×°ÖĆČēĶ¼ŅŅĖłŹ¾,ĘäÖŠµÄ¹ĢĢåµē½āÖŹŹĒY2O3-Na2O,O2-æÉŅŌŌŚĘäÖŠ×ŌÓÉŅĘ¶Æ”£ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ

A£®ĶßĖ¹·ÖĪöŅĒ¹¤×÷Ź±,µē³ŲÄŚµēĀ·ÖŠµē×ÓÓɵē¼«bĮ÷Ļņµē¼«a
B£®µē¼«bŹĒÕż¼«,O2-Óɵē¼«aĮ÷Ļņµē¼«b
C£®µē¼«aµÄ·“Ó¦Ź½ĪŖCH4+4O2--8e- CO2+2H2O
CO2+2H2O
D£®µ±¹ĢĢåµē½āÖŹÖŠÓŠ1 mol O2-ĶعżŹ±,µē×Ó×ŖŅĘ4 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓÄĻŹ”ø߶žÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ėĀ(N2H4)ŹĒ»š¼ż·¢¶Æ»śµÄČ¼ĮĻ£¬ĖüÓėN2O4·“Ó¦Ź±£¬N2O4ĪŖŃõ»Æ¼Į£¬Éś³ÉµŖĘųŗĶĖ®ÕōĘų”£ŅŃÖŖ£ŗ
N2(g)£«2O2(g)£½N2O4(g) ¦¤H£½£«8.7 kJ/mol£¬
N2H4(g)£«O2(g)£½N2(g)£«2H2O(g) ¦¤H£½£534.0 kJ/mol£¬
ĻĀĮŠ±ķŹ¾ėĀøśN2O4·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£¬ÕżČ·µÄŹĒ( )
A£®2N2H4(g)£«N2O4(g)£½3N2(g) £«4H2O(g) ¦¤H£½£542.7 kJ/mol
B£®2N2H4(g)£«N2O4(g)£½3N2(g)£«4H2O(g) ¦¤H£½£1059.3 kJ/mol
C£®N2H4(g)£« N2O4(g)£½
N2O4(g)£½ N2(g)£«2H2O(g) ¦¤H£½£1076.7 kJ/mol
N2(g)£«2H2O(g) ¦¤H£½£1076.7 kJ/mol
D£®2N2H4(g)£«N2O4(g)£½3N2(g)£«4H2O(g) ¦¤H£½£1076.7 kJ/mol
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com