
某pH=1的工业废液,只可能含有以下离子中的若干种:H+、Mg2+、Ba2+、Cl-、CO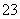 、SO
、SO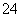 ,现取两份100 mL溶液进行如下实验:
,现取两份100 mL溶液进行如下实验:
第一份加入足量AgNO3溶液,得干燥沉淀3.50 g。
第二份加入足量BaCl2溶液后,得干燥沉淀2.33 g,经足量盐酸洗涤、干燥后,沉淀质量不变。
根据上述实验,以下推测正确的是 ( )
①一定存在Mg2+ ②可能存在CO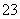 ③一定存在Cl- ④可能存在Ba2+ ⑤可能存在Mg2+
③一定存在Cl- ④可能存在Ba2+ ⑤可能存在Mg2+
A.①③ B.②③
C.③⑤ D.④⑤
科目:高中化学 来源: 题型:
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确的是
A.X为直流电源的负极,Y为直流电源的正极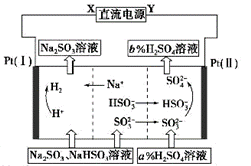
B.阳极区pH增大
C.图中的b>a
D.该过程中的产品主要为H2SO4和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定的溶液中,能大量共存的打“√”,不能大量共存的打“×”
(1)含有大量Fe3+的溶液:Na+、SCN-、Cl-、I- ( )
(2)含有大量NO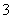 的溶液:H+、Fe2+、Cl-、SO
的溶液:H+、Fe2+、Cl-、SO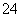 ( )
( )
(3)常温下,pH=12的溶液:K+、Cl-、SO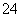 ( )
( )
(4)c(H+)=0.1 mol·L-1的溶液:Na+、NH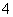 、SO
、SO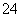 、S2O
、S2O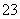 ( )
( )
(5)使pH试纸显蓝色的溶液:Cu2+、NO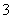 、Fe3+、SO
、Fe3+、SO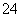 ( )
( )
(6)与铝粉反应放出H2的无色溶液:NO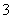 、Al3+、Na+、SO
、Al3+、Na+、SO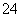 ( )
( )
(7)使红色石蕊试纸变蓝的溶液:SO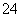 、CO
、CO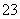 、Na+、K+ ( )
、Na+、K+ ( )
(8)常温下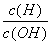 =1×10-12的溶液:K+、[Al(OH)4]-、CO
=1×10-12的溶液:K+、[Al(OH)4]-、CO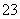 、Na+ ( )
、Na+ ( )
(9)中性溶液:Fe3+、Al3+、NO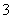 、SO
、SO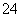 ( )
( )
(10)使甲基橙变红色的溶液:Mg2+、K+、SO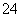 、SO
、SO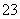 ( )
( )
(11)c(H+)水=10-12 mol·L-1的溶液:Na+、K+、CO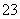 、SO
、SO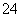 ( )
( )
(12)使酚酞变红色的溶液:Na+、Cu2+、Fe2+、NO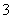 ( )
( )
(13)0.1 mol·L-1的Na2CO3溶液:Al3+、SO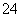 、Cl-、K+ ( )
、Cl-、K+ ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
在水溶液中能大量共存的一组离子是 ( )
A.Na+、Ba2+、Cl-、NO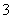
B.Pb2+、Hg2+、S2-、SO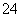
C.NH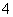 、H+、S2O
、H+、S2O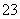 、PO
、PO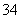
D.Ca2+、Al3+、Br-、CO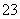
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能够大量共存,当溶液中c(H+)=10-1 mol·L-1时有气体产生;而 当溶液中c(H+)=10-13 mol·L-1时又能生成沉淀。则该组离子可能是 ( )
A.Na+、Ba2+、NO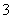 、CO
、CO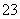
B.Ba2+、K+、Cl-、NO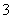
C.Mg2+、NH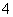 、SO
、SO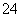 、Cl-
、Cl-
D.Fe2+、Na+、SO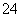 、NO
、NO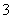
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关,下列说法不正确的是:
A.乙烯可作水果的催熟剂
B.硅胶可作袋装食品的干燥剂
C.褔尔马林可作食品的保鲜剂
D.氢氧化铝可作胃酸的中和剂
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
 (1)Y基态原子的电子排布式是① ;Z所在周期中第一电离能最大的元素是 ② 。
(1)Y基态原子的电子排布式是① ;Z所在周期中第一电离能最大的元素是 ② 。
(2)XY2- 离子的立体构型是 ① ;R2+的水合离子中,
提供孤电子对的原子是 ② 。
(3)将R单质的粉末加入XH3的浓溶液中,通入Y2,
充分反应后溶液呈深蓝色,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>cCH3COO-)>c(OH-)
B.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-)
C.0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合: c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D.0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H 2C2O4为二元弱酸):
2C2O4为二元弱酸):
2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池)。下列有关说法不正确的是:

A.放电时正极反应为:NiOOH+H2O+e-→Ni(OH)2+OH-
B.电池的电解液可为KOH溶液
C.充电时负极反应为:MH+OH-→+H2O+M+e-
D.MH是一类储氢材料,其氢密度越大,电池的能量密度越高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com