
| A、将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| B、盐酸中加入碳酸钙:CO32-+2H+═H2O+CO2↑ |
| C、铜片加入三氯化铁溶液中:Cu+2Fe3+═2Fe2++Cu2+ |
| D、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |


科目:高中化学 来源: 题型:
| A、HClO>Cl2>Fe3+>Cu2+>Fe2+ |
| B、Cl2>HClO>Fe3+>Cu2+>Fe2+ |
| C、Cl2>Fe3+>HClO>Cu2+>Fe2+ |
| D、HClO>Cl2>Cu2+>Fe3+>Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入一定量的CaCl2 |
| B、加入一定量的CaCO3 |
| C、加入15mL0.5mol/L的盐酸 |
| D、加入5mLH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制备Al2O3:将AlCl3溶液蒸干灼烧 |
| B、制备Fe(OH)3胶体:向沸水中滴加几滴FeCl3饱和溶液继续加热至红褐色 |
| C、检验溶液中是否含有CO32-:向某溶液中加入稀H2SO4,将产生的气体通入澄清石灰水 |
| D、比较CH3COO-和CO32-结合H+的能力强弱:相同温度下,测定浓度分别为0.1mol/L的Na2CO3和CH3COONa溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:
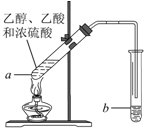 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
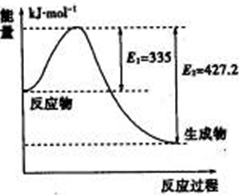 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
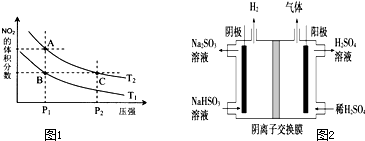
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com