
A、氢氧化钡溶液与稀硫酸:Ba2++2OH-+2H++SO
| ||
B、Al2(SO4)3浴液中加入足量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH
| ||
| C、FeBr2溶液中通入过量Cl2 2Fe2++6Br-+4Cl2=2Fe3++3Br2+8Cl- | ||
| D、Fe2O3溶于过量的盐酸中:Fe2O3+6H+=2Fe3++3H2O |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、Na+、NH4+、Fe2+、NO3-(稀硫酸) |
| B、Al3+、K+、HCO3-、NO3-(NaOH溶液) |
| C、NH4+、Ag+、K+、NO3-(NaOH溶液) |
| D、Na+、K+、AlO2-、SiO32-(稀硝酸) |
查看答案和解析>>
科目:高中化学 来源: 题型:
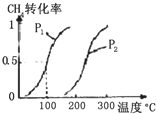 甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.
甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.| 实验编号 | T(°C) | n(CO)/n(H2) | p(MPa) | ||
| I | 150 |
|
0.1 | ||
| II | 5 | ||||
| III | 350 | 5 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X(g)+Y(g)?2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法错误的是( )
如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X(g)+Y(g)?2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法错误的是( )| A、反应开始时,B容器中化学反应速率快 |
| B、A容器中X的转化率为40%,且比B容器中X的转化率大 |
| C、打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计) |
| D、打开K达新平衡后,升高B容器温度,A容器体积一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用阳离子交换膜法电解饱和食盐水制取烧碱 |
| B、将黏土和石灰石研磨成粉末,再混合均匀即可得普通水泥 |
| C、目前合成氨,没有采用更大压强是从设备和动力要求方面考虑的 |
| D、生产硫酸时,接触室内热交换器的作用是预热进入的炉气和冷却反应生成的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com