
【题目】X、Y、Z、R为前四周期原子序数依次增大的元素。X原子有3个能级,且每个能级上的电子数相等;Z原子的不成对电子数在同周期中最多,且Z的气态氢化物在同主族元素的氢化物中沸点最低;X、Y、R三元素在周期表中同族。
(1)R元素在周期表中的位置是_______________________,其基态原子的价层电子排布图为__________________________。
(2)下图表示X、Y、Z的四级电离能变化趋势,其中表示Z的曲线是_________(填标号)。

(3)化合物(XH2=X=O)分子中X原子杂化轨道类型是___________,1mol (X2H5O)3Z=O分子中含有的σ键与π键的数目比为_______________。
(4)Z与氯气反应可生成一种各原子均满足8电子稳定结构的化合物,其分子的空间构型为______。
(5)某R的氧化物晶胞结构如下图所示,该物质的化学式为____________。已知该晶体密度为ρg/cm3,距离最近的两个原子的距离为d pm,则R的相对原子质量为___________________。 (阿伏加德罗常数为NA)

(6)X形成的一种常见单质,性质硬而脆,原因是____________________。
【答案】 第四周期,ⅣA族 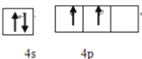 b sp、sp2 25:1 三角锥形 GeO (
b sp、sp2 25:1 三角锥形 GeO (![]() )3×ρ×
)3×ρ×![]() ×NA-16 碳碳键键能大,故硬;但共价键有方向性,受大的外力时,会发生原子错位而断裂,故脆
×NA-16 碳碳键键能大,故硬;但共价键有方向性,受大的外力时,会发生原子错位而断裂,故脆
【解析】X原子有3个能级,且每个能级上的电子数相等,电子排布式为1s22s22p2,推出X为C,因为X、Y、R三元素在周期表同族,因此Y为Si,R为Ge,原子序数依次增大,Z原子的不成对电子数在同周期中最多,且Z的气态氢化物在同主族元素的氢化物中沸点最低,因此Z为P,(1)Ge位于第四周期第IVA族,因为是主族元素,因此价电子是最外层电子,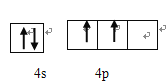 ;(2)本题考查电离能的规律,同主族从上到下第一电离能减小,P元素3p能级为半满稳定状态,第一电离能高于同周期相邻元素,故Si的第一电离能最小,P原子第四电离能为失去4s2能中的1个电子,为全满稳定状态,与第三电离能相差较大,因此b曲线为P;(3)本题考查杂化类型、化学键的判断,CH2=C=O中“CH2=”中的碳原子有3个σ键,无孤电子对,因此杂化类型为sp2,“C=O”中的C有2个σ键,无孤电子对,杂化类型为sp;成键电子对之间只能形成一个σ键,双键中有一个π键,因此σ键和π键的数目比值为25:1;(4)本题考查空间构型,P和氯气反应生成PCl3和PCl5,均满足8电子结构的是PCl3,中心原子是P,有3个σ键,孤电子对数为(5-3)/2=1,因此空间构型为三角锥形;(5)本题考查晶胞的结构,氧原子位于顶点和面心,个数为8×1/8+6×1/2=4,Ge全部位于晶胞内部,因此化学式为GeO,晶胞的质量为4×(M+16)/NAg,距离最近的两个原子是体对角线的1/4,因此体对角线为4d,则边长为
;(2)本题考查电离能的规律,同主族从上到下第一电离能减小,P元素3p能级为半满稳定状态,第一电离能高于同周期相邻元素,故Si的第一电离能最小,P原子第四电离能为失去4s2能中的1个电子,为全满稳定状态,与第三电离能相差较大,因此b曲线为P;(3)本题考查杂化类型、化学键的判断,CH2=C=O中“CH2=”中的碳原子有3个σ键,无孤电子对,因此杂化类型为sp2,“C=O”中的C有2个σ键,无孤电子对,杂化类型为sp;成键电子对之间只能形成一个σ键,双键中有一个π键,因此σ键和π键的数目比值为25:1;(4)本题考查空间构型,P和氯气反应生成PCl3和PCl5,均满足8电子结构的是PCl3,中心原子是P,有3个σ键,孤电子对数为(5-3)/2=1,因此空间构型为三角锥形;(5)本题考查晶胞的结构,氧原子位于顶点和面心,个数为8×1/8+6×1/2=4,Ge全部位于晶胞内部,因此化学式为GeO,晶胞的质量为4×(M+16)/NAg,距离最近的两个原子是体对角线的1/4,因此体对角线为4d,则边长为![]() pm,晶胞的体积为(
pm,晶胞的体积为(![]() ×10-10)3,根据晶胞的密度,求出M,则M=(
×10-10)3,根据晶胞的密度,求出M,则M=(![]() )3×ρ×
)3×ρ×![]() ×NA-16;(6)碳碳键键能大,故硬;但共价键有方向性,受大的外力时,会发生原子错位而断裂,故脆。
×NA-16;(6)碳碳键键能大,故硬;但共价键有方向性,受大的外力时,会发生原子错位而断裂,故脆。


科目:高中化学 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4 制备路线如下:

查阅资料:
I.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡[Sn(OH)C1]。
回答下列问题:
(1)操作I的步骤为_____________________、过滤、洗涤、干燥。过滤后滤液仍混浊的原因是(除滤纸破损,所有仪器均洗涤干净)__________________________、__________________________.
(2)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式及化学反应原理解释原因:
_________________________________________________
(3)加入锡粉的作用有两个:①调节溶液pH;②_____________________。
(4)SnS04还可在酸性条件下用作双氧水的去除剂,发生反应的离子方程式是______________________________________。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取质量为m g的锡粉溶于稀硫酸中,向生成的SnSO4中加入过量的Fe2(SO4)3溶液,用物质的量浓度为c mol/L的K2Cr207标准溶液滴定生成的Fe2+,共用去K2Cr207溶液的体积为V L。 则锡粉中锡的质量分数是_______________。(Sn的摩尔质量为M g/mol,用含m、c、V、M的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖,其晶胞结构如图。

(1)根据图示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,确定其化学式_________________。
(2)根据(1)所推出的化合物的组成,计算其中Cu原子的平均化合价(该化合物中各元素的化合价为![]() 、
、![]() 、
、![]() 和
和![]() ),试计算化合物中这两种价态Cu原子个数比___________。
),试计算化合物中这两种价态Cu原子个数比___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】埋在地下的铸铁输油管道,在下列各种情况下,被腐蚀速率最慢的是
A. 在含铁元素较多的酸性土壤中 B. 在潮湿疏松的碱性土壤中
C. 在干燥致密不透气的土壤中 D. 在含碳粒较多,潮湿透气的中性土壤中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物——合金。这是制取合金的常用方法之一。根据下表数据判断,不宜用上述方法制取合金的是( )
金属 | Na | Al | Cu | Fe |
熔点(℃) | 97.81 | 660 | 1 083 | 1 535 |
沸点(℃) | 883 | 2 200 | 2 595 | 3 000 |
A. Fe-Cu合金 B. Cu-Al合金 C. Al-Na合金 D. Cu-Na合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了保护环境,充分利用资源,可将工业废弃物转变成重要的化工原料。
请回答下列问题:
(1)可用NaClO3氧化酸性FeCl2废液得到FeCl3,FeCl3具有净水作用,但腐蚀设备。
①写出NaClO3氧化酸性FeCl2的离子方程式:__________________________。
②若酸性FeCl2废液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,则该溶液的pH约为_________。
③FeCl3净水的原理是:_________________(用离子方程式及适当文字回答);FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是_________(用离子方程式表示)。
(2)可用废铁屑为原料,按下图的工艺流程制备聚合硫酸铁(PFS),PFS是一种新型的
絮凝剂,处理污水比FeCl3高效,且腐蚀性小。
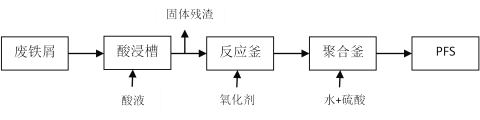
①酸浸时最合适的酸是______________。
②反应釜中加入的氧化剂,下列试剂中最合适的是____________(填标号)。
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
检验其中Fe2+是否完全被氧化,应选择____________________(填标号)。
a.K3[Fe(CN)6]溶液 b.Na2SO3溶液 c.KSCN溶液
③生成PFS的离子方程式为:xFe3++yH2O Fex(OH)y(3x-y)++yH+欲使平衡正向移动可采用的方法是____________(填标号)。
a.加入NaHCO3 b.降温 c.加水稀释 d.加入NH4Cl
(3)废铁屑在一定条件下,可制得FeS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li+FeS2=Fe+2Li2S,维持电流强度为1A,a电池工作1小时,理论上消耗FeS2__________g。(已知1mol电子的电量为96500C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在粗盐提纯的实验中,蒸发时正确的操作是( )
A. 把浑浊的液体倒入蒸发皿内加热
B. 蒸发皿中发现有大量固体析出时即停止加热
C. 开始有固体析出后使用玻璃棒搅拌
D. 待水分完全蒸干后停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
A. 使红色布条褪色(HCl)
B. 将NaHCO3固体加入新制氯水,有无色气泡(H+)
C. 向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)
D. 滴加AgNO3溶液生成白色沉淀(Cl-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com