
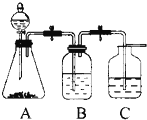
 为了确定HCl、C6H5OH及H2CO3的酸性强弱,有人设计了如图所示的装置进行实验:
为了确定HCl、C6H5OH及H2CO3的酸性强弱,有人设计了如图所示的装置进行实验:

科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 无明显现象 |
| ② | B+D | 有无色无味气体放出 |
| ③ | C+B | 有白色沉淀生成 |
| ④ | A+D | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省舟山市岱山县大衢中学高二(上)期中化学试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com