
 (g)Si(s)+4HCl(g) △H =Q(Q>O),某温度、压强下,将一定量的反应物通入密闭容器进行以上反应,下列叙述正确的是
(g)Si(s)+4HCl(g) △H =Q(Q>O),某温度、压强下,将一定量的反应物通入密闭容器进行以上反应,下列叙述正确的是  中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
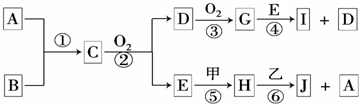
| 2 |
| 3 |
| 2 |
| 3 |
| ||
| 冰晶石 |
| ||
| 冰晶石 |
查看答案和解析>>
科目:高中化学 来源: 题型:
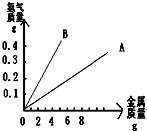 金属和非金属与人类生活、生产密不可分.
金属和非金属与人类生活、生产密不可分.
| ||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年贵州省湄潭中学高二上学期期中考试化学试卷(带解析) 题型:单选题
工业上制备纯硅的反应为:SiCl4(g)+2H2(g) Si(s)+4HCl(g)△H=+236kJ/mol,将一定量反应物通入密闭容器进行以上可逆反应,既能提高SiCl4的转化率又能缩短达到平衡的时间的是
Si(s)+4HCl(g)△H=+236kJ/mol,将一定量反应物通入密闭容器进行以上可逆反应,既能提高SiCl4的转化率又能缩短达到平衡的时间的是
| A.增大压强 | B.减小氢气浓度 | C.升高温度 | D.加入催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com