
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为 ;XW的电子式为 ;
(2)Z元素在周期表中的位置是 ;
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式) ;
(4)写出X的单质在UW2中燃烧的化学方程式,并表示电子的转移方向和数目为 。
(1)N≡N  (2) 第4周期,第Ⅷ族
(2) 第4周期,第Ⅷ族
(3)CH4
(4)2Mg+CO2=2MgO+C(写成双线桥或者单线桥均可)
解析试题分析:Y的单质在W2中燃烧的产物可使品红溶液褪色.该气体为SO2,则Y为S元素,W为O元素,Z和W元素形成的化合物Z3W4具有磁性,则Z3W4为Fe3O4,Z为Fe元素,U的单质在W2中燃烧可生成UW和UW2两种气体,应为CO和CO2气体,U为C元素,X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体,应为Mg和CO2的反应,则X为Mg元素,根据U、V、W、X、Y、Z是原子序数依次增大可知V为N元素,(1)V为N元素,其单质为N2,结构为N≡N,;XW为MgO,为离子化合物,电子式为 ,(2)Z为Fe元素,原子序数为26,位于元素周期表中第四周期,第VIII族,故答案为:N≡N;
,(2)Z为Fe元素,原子序数为26,位于元素周期表中第四周期,第VIII族,故答案为:N≡N; ;第四周期,第VIII族.(3)U、V、W形成的10电子氢化物分别是CH4、NH3、H2O,NH3含有氢键,沸点比甲烷的沸点高,故答案为:CH4;(4)2Mg+CO2=2MgO+C(写成双线桥或者单线桥均可)
;第四周期,第VIII族.(3)U、V、W形成的10电子氢化物分别是CH4、NH3、H2O,NH3含有氢键,沸点比甲烷的沸点高,故答案为:CH4;(4)2Mg+CO2=2MgO+C(写成双线桥或者单线桥均可)
考点:本题考查元素推断题,题目较为综合,涉及电子式、晶体类型、氢键以及氧化还原反应等问题。


科目:高中化学 来源: 题型:填空题
短周期元素X、Y、Z、W原子序数依次增大。X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是常见的非金属元素,主要以钠盐的形式存在于海水中。
(1)Y在元素周期表中的位置是________;X氢化物的电子式为_________。
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈_______(填“酸”、“碱”或“中”)性,用离子方程式表示其原因是________。
(3)Y-Ag2O电池是应用广泛的鱼雷电池,其原理如下图所示。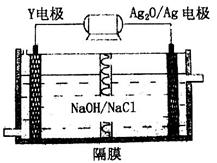
该电池的负极反应式是________。
(4)Z和W比较,非金属性较弱的是________(填元素符号),下列可以验证这一结论的是_________
(填序号)。
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H—Z或H—W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
短周期元素X、Y、Z、W原子序数依次增大。X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中。请回答:
(1)X氢化物的电子式是_________________________________________。
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈(填“酸”、“碱”或“中”)性,用离子方程式表示其原因是_____________________________________.
(3)Y—AgO电池是应用广泛的鱼雷电池,其原理如图所示。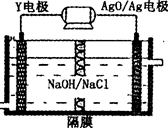
该电池的负极反应式是___________________________________。
(4)Z和W比较,非金属性较弱的是_______________(填元素符号),下列不能验证这一结论的是________(填序号)。
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1 mol H—Z或H—W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别是同一主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,又知四种元素的单质中有两种气体、两种固体。
(1) A ;D (填元素名称)
(2)写出C、D两元素形成的常见化合物的电子式 ;写出由A、B两元素形成的18电子微粒中所含化学键类型 。
(3)用A元素的单质与B元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特制的防止气体透过的隔膜。在一极通人A的单质,另一极通人B的单质,写出该电池发生的电极反应式:
通入A单质的一极: ;
通入B单质的一极: 。
(4)由A、B、C 三元素构成的化合物X,常在试验制备过程中起尾气吸收作用。请写出化合物X吸收NO2 时所发生反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有X、Y、Z、W四种元素,它们的单质X、Y、Z在常温常压下皆为气体,W为固体。
①X单质可在Z单质中燃烧生成XZ,其火焰为苍白色;W单质在Y单质中剧烈燃烧产生黄色火焰,生成W2Y2;
②每2molX2可与1molY2化合生成2molX2Y,X2Y在常温下为液体;
③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红色;
④Z单质溶于化合物X2Y,所得溶液具有漂白作用;请回答:
(1)画出Z原子的原子结构示意图 ;实验室中的W应保存在____________中(填试剂名称)
(2)写出化学式W2Y2___________ _K#S5U
(3)写出与W+具有相同核外电子数的分子或原子,请写出任意3种的化学式
① ② ③
(4)Z单质与水反应的离子方程式:_________________________
⑸W单质与X2Y化学反应方程式:__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表为元素周期表的一部分,其中编号代表对应的元素。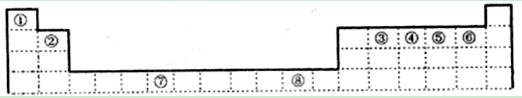
请回答下列问题:
(1)写出元素⑦的基态原子外围电子排布式 ,元素⑧位于 区。
⑤元素原子的价层电子的轨道表示式为 ,
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,该化合物对氢气的相对密度为23,则其中所有杂化原子的杂化方式分别为 和 。
(3)元素③④⑤⑥的第一电离能由大到小的顺序是 (用元素符号表示)。请写出由④和⑤两种元素形成的与N3ˉ互为等电子体的分子的化学式 ,
(写出一种即可)其VSEPR构型为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
根据表中信息回答下列问题。
| 元素 | Si | P | S | Cl |
| 单质与氢气 反应的条件 | 高温 | 磷蒸气与氢气能反应 | 加热 | 光照或点燃时发生爆炸而化合 |
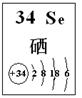
| 编号 | 性质推测 | 化学方程式 |
| 1 | 氧化性 | H2SeO3+4HI=Se↓+2I2+3H2O |
| 2 | | |
| 3 | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y的最高正价与最低负价的代数和为2,Z与X原子最处层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为 、 、_ 。
(2)选用以上元素组成一种离子化合物,该化合物为______ 。
(3)X和Y组成的化合物Q中,既含有极性共价键又含有非极性共价键,Q的分子式是 。Q在空气中点燃时,迅速而安全的燃烧,其反应产物没有任何污染,燃烧时的化学方程式为 ;Q还可将酸性工业废水中的Cr2O72-还原为Cr3+,氧化产物为常见气体。相应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
回答以下关于第三周期元素及其化合物的问题。
(1)Na原子核外共有 种不同运动状态的电子,有 种不同能量的电子。
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com