
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式______________________________、________________________________。
(2)甲水浴的作用是_________________________________________;乙水浴的作用是_________________________________________。
(3)反应进行一段时间后,干试管a中能收集到不同的物质,它们是________。集气瓶中收集到的气体的主要成分是________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有______。要除去该物质,可在混合液中加入____________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
【答案】2Cu+O2![]() 2CuO CH3CH2OH+CuO
2CuO CH3CH2OH+CuO![]() CH3CHO+Cu+H2O 加热,使乙醇气化 冷却,使乙醛等液化 乙醛、乙醇、水 氮气 乙酸 c
CH3CHO+Cu+H2O 加热,使乙醇气化 冷却,使乙醛等液化 乙醛、乙醇、水 氮气 乙酸 c
【解析】
甲中鼓入空气,且在水浴加热条件下产生乙醇蒸汽,氧气和乙醇在铜催化下加热发生氧化还原反应生成乙醛和水,进入乙中的为乙醇、乙醛,在冷却下收集到乙醛,集气瓶收集氮气,据此解答。
(1)加热条件下铜和氧气反应生成氧化铜,氧化铜又氧化乙醇生成乙醛、铜和水,因此实验过程中铜网出现黑色和红色交替的现象,相应的化学方程式分别是2Cu+O2![]() 2CuO、CH3CH2OH+CuO
2CuO、CH3CH2OH+CuO![]() CH3CHO+Cu+H2O。
CH3CHO+Cu+H2O。
(2)常温下乙醇是液体,参加反应的是乙醇蒸汽,则甲水浴的作用是加热,使乙醇气化;生成物乙醛是液体,则乙水浴的作用是冷却,使乙醛等液化。
(3)由于是连续反应,乙醇不能完全被消耗,则反应进行一段时间后,干试管a中能收集到的物质是乙醛、乙醇、水。空气中含有氮气不参与反应,则集气瓶中收集到的气体的主要成分是氮气。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明显酸性,因此液体中还含有乙酸。四个选项中只有碳酸氢钠能与乙酸反应,则要除去该物质,可在混合液中加入碳酸氢钠溶液,答案选c。


科目:高中化学 来源: 题型:
【题目】下列是几则广告语,请判断在上述广告语中,有多少条在科学性上有明显的错误?
①这种食品由纯天然谷物制成,不含任何糖类,糖尿病患者也可放心大量食用
②这种饮料含有多种无机盐,能有效补充人体运动时消耗的能量
③这种矿泉水含有人体所需的部分大量元素和微量元素
④这种口服液含有丰富的钙、铁、锌、硒等微量元素
A. 1条 B. 2条 C. 3条 D. 4条
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象不能说明浓硫酸具有强氧化性的是
A.能用铝槽车运输浓硫酸
B.浓硫酸能与不活泼金属在加热条件下反应
C.浓硫酸滴到白纸上,使白纸变黑
D.不活泼非金属单质能与浓硫酸反应生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知:反应aA(g)+bB(g)cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。

(1)经测定前4 s内v(C)=0.05 mol·L1·s1,则该反应的化学方程式为______________。
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L1·s1;乙:v(B)=0.12 mol·L1·s1;丙:v(C)=9.6 mol·L1·min1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为___________(用甲、乙、丙表示)。
Ⅱ.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
编号 | 操作 | 实验现象 |
① | 分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入1~2 滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5 ℃左右冷水的烧杯中;将试管B放入盛有40 ℃左右热水的烧杯中 | 试管A中不再产生气泡试管B中产生的气泡量增大 |
② | 另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 | 试管A、B中均未见气泡产生 |
(3)实验①的目的是_______________________________,实验中滴加FeCl3溶液的目的是____________________________。
(4)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是______________________________________________________________(用实验中所提供的几种试剂)。

(5)某同学在50 mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如右图所示,则A、B、C三点所表示的即时反应速率最慢的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛋白质的生理作用包括 ( )
①构成染色体 ②构成生物膜 ③是人体主要的能源物质 ④构成多种酶 ⑤组成所有激素 ⑥参与体液免疫过程
A. ①②③④B. ①②④⑤C. ②③④⑤D. ①②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是( )
A. 甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. 500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ·mol-1(120 ℃、101 kPa)
D. 25 ℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热ΔH为-57.3 kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l) ΔH=-57.3 kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
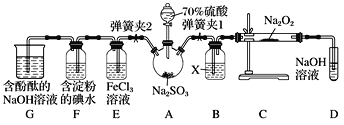
(1)在组装好装置后,若要检验A~D装置的气密性,其操作是首先__________,然后往D中装入水,然后微热A,观察到D中有气泡冒出,移开酒精灯或松开双手,D中导管有水柱形成且高度保持不变,说明装置气密性良好。
(2)装置D中盛放NaOH溶液的作用是___________。
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为_____;发生反应的离子方程式是________________。
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应。
上述方案是否合理?________(填“合理”或“不合理”),原因是_____________。
(5)实验过程中G中含酚酞的NaOH溶液逐渐褪色,此实验证明SO2具有漂白性还是其溶于水显酸性?请设计实验验证:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2A(g)![]() 2B(g)+E(g) ΔH>0,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
2B(g)+E(g) ΔH>0,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
A. 加压 B. 升温 C. 减少E的浓度 D. 降温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是某种药物合成的中间体,其合成路线如下:
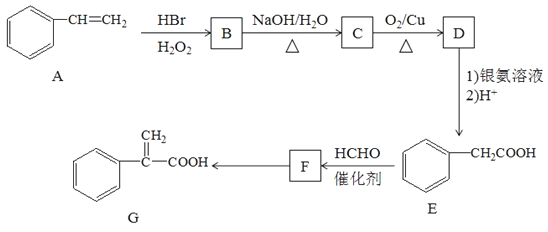
已知:①CH3-CH=CH2+HBr![]() CH3-CH2-CH2Br
CH3-CH2-CH2Br
②CH3COOH+HCHO![]() HOCH2CH2COOH
HOCH2CH2COOH
请回答下列问题:
(1)A的名称为___________________________。
(2)F中官能团名称是______________________________;E转化F的反应类型是_________________。
(3)F转化为G的化学方程式:_________________________________________。
(4)化合物F有多种同分异构体,满足下列条件的同分异构体有__________种。
①属于芳香族化合物且苯环上有两个取代基;
②能发生水解反应和银镜反应;
③与FeCl3溶液发生显色反应。
其中核磁共振氢谱图有6组峰且峰面积之比为1:2:2:2:2:1的有机物的结构简式为__________________;
(5)参照上述合成路线设计一条由CH3CHBrCH3和C2H5OH制备CH3CH2COOC2H5的合成路线(其他试剂自选)______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com