
α1和α2,c1和c2分别为两个恒容容器中平衡体系N2O4(g) 2NO2(g)和3O2(g)
2NO2(g)和3O2(g) 2O3(g)的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应物的物质的量,下列判断正确的是
2O3(g)的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应物的物质的量,下列判断正确的是
A.α1、α2均减小,c1、c2均增大
B.α1、α2均增大,c1、c2均减小
C.α1减小,α2增大,c1、c2均增大
D.α1减小,α2增大,c1增大,c2减小
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:2016-2017学年福建省三明市高一上期中化学试卷(解析版) 题型:选择题
下列实验设计方案中,可行的是( )
A.用加入适量铜粉的方法除去Mg(NO3)2溶液中混有的AgNO3
B.用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体
C.向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO42-
D.先滴加石蕊试液,后滴加BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上学期期中化学试卷(解析版) 题型:选择题
丙酮(C3H60)通常是无色液体,易溶于水,密度小于1g/mL,沸点约为55℃。要从水与丙酮的混合物中将丙酮分离出来,你认为下列方法中最为合理的是( )
A.蒸馏 B.分液 C.过滤 D.蒸发
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上月考四化学试卷(解析版) 题型:选择题
我国有广阔的海岸线,建设海峡经济区,海水的综合利用大有可为,下图所示为海水综合利用部分流程,有关说法正确的是( )
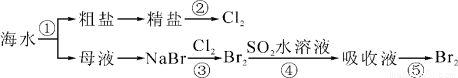
A.上述工艺流程中涉及到化合、分解、复分解和置换反应
B.①只发生了化学变化,②是工业上用电解熔融NaCl制备Cl2
C.③④涉及的反应均为氧化还原反应,⑤只需要蒸馏即可得到单质Br2
D.④中反应的离子方程式为SO2+Br2+2H2O===4H++SO42-+2Br-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市六校高二上学期期中化学卷(解析版) 题型:实验题
定量分析是化学实验中重要的组成部分。
Ⅰ.中和热的测定:
(1)在实验室中,用50 mL 0.40 mol/L的盐酸与50 mL 0.50mol/L的NaOH溶液反应测定和热。假设此时溶液密度均为1 g/cm3,生成溶液的比容热c = 4.18 J/(g•℃),实验起始温度为T1℃,终止温度为T2℃,请写出中和热的计算式(写出最后结果)△H=__________KJ/mol。
(2)1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6 kJ的热量。请写出表示该反应中和热的热化学方程式 。
Ⅱ.氧化还原滴定实验与中和滴定类似。为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L KMnO4标准溶液滴定。
(1)滴定原理为: (用离子方程式表示)。
(2)滴定时,KMnO4溶液应装在 (填“酸式”或“碱式”)滴定管中,达到滴定终点时的颜色变化为 。
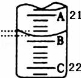
(3)如图表示50mL滴定管中液面的位置,此时滴定管中液面的读数为 mL。
(4)为了减小实验误差,该同学一共进行了三次实验,假设每次所取H2C2O4溶液体积均为VmL,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗KMnO4溶液体积/mL | 26.32 | 24.02 | 23.98 |
从上表可以看出,第一次实验中记录消耗KMnO4溶液的体积明显多于后两次,其原因可能是 。
A.实验结束时俯视刻度线读取滴定终点时KMnO4溶液的体积
B.滴加KMnO4溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.第一次滴定盛装标准液的滴定管装液前用蒸馏水清洗过,未用标准液润洗,后两次均用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
(5)写出计算H2C2O4的物质的量浓度的最简表达式:C= mol/L。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市六校高二上学期期中化学卷(解析版) 题型:选择题
已知反应mX(g)+nY(g) qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.增加X的物质的量,Y的转化率降低
C.降低温度,混合气体的平均相对分 子质量变小
子质量变小
D.X的正反应速率是Y的逆反应速率的m/n倍
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市六校高二上学期期中化学卷(解析版) 题型:选择题
一定条件下,某容积不变的密闭容器内存在下列平衡:2HI(g) H2(g)+I2(g);则下列有关说法正确的是
H2(g)+I2(g);则下列有关说法正确的是
A.如改变体系温度,体系颜色一定发生变化
B.如仅仅改变浓度这一条件,使得体系颜色加深,则上述平衡一定正移
C.继续充入HI气体,则HI的转化率将减小
D.温度不变时 ,当体系颜色变浅,则正反应速率和逆反应速率都将减小
,当体系颜色变浅,则正反应速率和逆反应速率都将减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市五县七校高一上期中化学试卷(解析版) 题型:填空题
A.氢氧化铝胶体;
B.食盐水;
C.铜;
D.硝酸;
E.烧碱;
F.蔗糖;
G.泥水;
H.一氧化碳;
I.CuSO4·5H2O晶体;
J.SO2;
K.HCl 气体;
L.CaO固体;
M.食醋(含醋酸的溶液)
(1)下列物质中属于电解质的是 (填序号,下同);属于非电解质的是 。
(2)上述的酸性氧化物与氢氧化钠反应的化学方程式为 ,上述的碱性氧化物与盐酸反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市五县七校高二上期中化学试卷(解析版) 题型:选择题
下列反应过程能量变化如下所示:
H2(g)+Cl2(g)=2HCl(g)ΔH
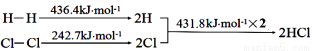
下列说法错误的是
A.H—H键比Cl—Cl键稳定
B.正反应活化能比逆反应活化能高
C.ΔH= — 184.5 kJ·mol-1
D.在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时ΔH相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com