
(10分)蛇纹石可用于生产氢氧化镁,简要工程如下:
Ⅰ.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤,并在常温常压下结晶,制得粗硫酸镁(其中常含有少量Fe3+、Al3+、Fe2+等杂质离子)
Ⅱ.提纯粗硫酸镁,将粗硫酸镁在酸性条件下溶解,加入适量的0.1mol/LH2O2溶液,再调节溶液pH至7~8,并分离提纯。
Ⅲ.制取氢氧化镁,向步骤II所得溶液中加入过量氨水。
已知:金属离子氢氧化物沉淀所需pH
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
请回答:
(1)步骤II中加入适量的0.1mol/LH2O2溶液的目的是 ;可用于调节溶液pH至7~8的最佳试剂是 (填字母序号)
A.MgO B.Na2CO3 C.蒸馏水 D.NaOH .
(2)工业上常以Mg2+的转化率为考查指标,确定步骤III制备氢氧化镁工艺过程的适宜条件。
其中,反应温度与Mg2+转化率的关系如图所示。
①步骤III中制备氢氧化镁反应的离子方程式为 。根据图中所示50℃前温度与Mg2+转化率之间的关系,可判断此反应是 (填“吸热”或“放热”反应)
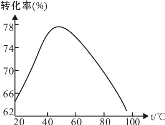
②图中,温度升高至50℃以上Mg2+转化率下降的可能原因是 。
(1)将Fe2+氧化成Fe3+ ;A ;
(2) ①Mg2+ + 2NH3·H2O  Mg(OH) 2↓+ 2NH4+;吸热
Mg(OH) 2↓+ 2NH4+;吸热
②温度过高时,氨水受热分解,浓度降低,使Mg2+转化率降低。
【解析】
试题分析:(1)步骤II中加入适量的0.1mol/LH2O2溶液的目的是将Fe2+氧化成Fe3+ ; 加入的试剂应该是只调节溶液的pH ,但是不能引入新的杂质离子。可用于调节溶液pH至7~8的最佳试剂是MgO ,选项是A;(2)①向含有Mg2+的溶液中加入氨水,发生反应制备氢氧化镁,步骤III中反应的离子方程式为Mg2+ + 2NH3·H2O  Mg(OH) 2↓+ 2NH4+;在50℃前温度越高,物质的转化率越高。根据平衡移动原理:升高温度,平衡向吸热反应方向移动,证明正反应是吸热反应;②图中,温度升高至50℃以上Mg2+转化率下降的可能原因是温度过高时,氨水受热分解,浓度降低,使Mg2+转化率降低。
Mg(OH) 2↓+ 2NH4+;在50℃前温度越高,物质的转化率越高。根据平衡移动原理:升高温度,平衡向吸热反应方向移动,证明正反应是吸热反应;②图中,温度升高至50℃以上Mg2+转化率下降的可能原因是温度过高时,氨水受热分解,浓度降低,使Mg2+转化率降低。
考点:考查物质的作用、反应条件的控制、化学平衡移动原理在物质的吸收中的作用及温度对物质吸收率的影响的知识。


科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:选择题
工业上以CuFeS2为原料冶炼铜的主要反应为①2CuFeS2+4O2 Cu2S+3SO2+2FeO(炉渣);
Cu2S+3SO2+2FeO(炉渣);
②2Cu2S+3O2 2Cu2O+2SO2;③2Cu2O+Cu2S
2Cu2O+2SO2;③2Cu2O+Cu2S 6Cu+SO2↑。下列说法错误的是( )
6Cu+SO2↑。下列说法错误的是( )
A.由1 mol CuFeS2生成1mol Cu,共消耗2.75 molO2
B.该冶炼方法中产生大量的有害气体SO2,可回收用于制备硫酸
C.在反应③中,Cu2S既是氧化剂,又是还原剂
D.在反应①中,SO2既是氧化产物,又是还原产物
查看答案和解析>>
科目:高中化学 来源:2015届河南省高三9月第二次阶段考化学试卷(解析版) 题型:选择题
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸D.若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期期中理综化学试卷(A)(解析版) 题型:填空题
(14分)工业上用铝土矿(主要成分为Al2O3,Fe2O3等)提取Al2O3作冶炼铝的原料,由熔盐电解法获得的粗铝中含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下图所示:
(已知:NaCl熔点为801℃;AlCl3在181℃升华)

(1)赤泥中的主要成分是 (化学式);向滤液中通入过量CO2所发生反应的离子方程式为 。
(2)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,则铝和氧化铁反应的化学方程式为 。
(3)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮而除去。气泡的主要成分除Cl2外还含有______。固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在________。
(4)镀铝电解池中,金属铝为阳极,熔融盐电镀液中铝元素主要以AlCl4-形式存在,则阳极的电极反应式为_____________。
(5)钢材镀铝后,抗腐蚀性能会大大增强,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期期中理综化学试卷(A)(解析版) 题型:选择题
工业上可用硫酸铝与硫黄焙烧制备氧化铝:2Al2(SO4)3+3S  2Al2O3+9SO2↑,下列有关说法中正确的是
2Al2O3+9SO2↑,下列有关说法中正确的是
A.反应中Al2(SO4)3被氧化
B.Al2O3是氧化产物
C.该反应中,每转移0.3 mol电子生成5.04 L SO2
D.氧化产物与还原产物的质量之比为1︰2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:选择题
通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热△H为
Si(s)+4HCl(g),该反应的反应热△H为
A.+236 kJ·mol-1 B.-236 kJ·mol-1
C.+412 kJ·mol-1 D.-412 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:选择题
高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O===3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述正确的是
A.放电时,负极反应式为3Zn-6e-+6OH-===3Zn(OH)2
B.放电时,正极区溶液的pH减小
C.充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原
D.充电时,电池的锌电极接电源的正极
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省莆田市高三上学期第二次月考化学试卷(解析版) 题型:实验题
(14分)亚硝酸钠(NaNO2)是一种外观与食盐相似的食品添加剂。兴趣小组用如下装置制NaNO2 (夹持和加热装置已省略)。已知:2NO+Na2O2 = 2NaNO2;2NO2+Na2O2 = 2NaNO3。
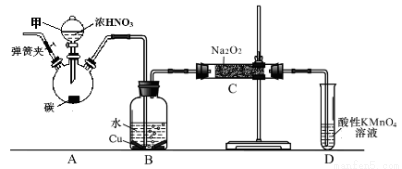
(1)仪器甲的名称是__ _;装置A烧瓶中发生反应的化学方程式为 。
(2)B装置的作用是 。
写出所发生主要反应的化学方程式① ;② ___________ 。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为排除干扰应在B、C装置间增加装置E,E中盛放的试剂应是 (填字母)。
A.浓H2SO4 B.碱石灰 C.无水CaCl2
(4)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为____ _________。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:填空题
(选做题12分)
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO4·7H2O。
Ⅱ.将FeSO4·7H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeC03的浊液。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeC03固体。
ⅴ.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是 。
(2)Ⅱ中,需加一定量硫酸。运用化学平衡原理简述硫酸的作用 。
(3)Ⅲ中,生成FeCO3的离子方程式是 。若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式 。
(4)IV中,通过检验SO42-来判断沉淀是否洗涤干净。检验SO42的操作是 。
(5)已知煅烧FeC03的化学方程式是4FeCO3+O2  2Fe2O3+4CO2。现煅烧464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是 Kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
2Fe2O3+4CO2。现煅烧464.0 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是 Kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com