
【题目】Ⅰ.某化学学习小组为探究NO2和SO2的反应进行如图所示实验。
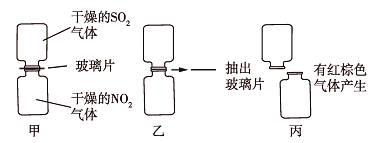
(1)图甲两集气瓶中__(填“上”或“下”)瓶气体颜色深。
(2)图乙中反应的现象是___。
(3)图丙中“有红棕色气体产生”说明SO2和NO2反应的产物中有__,NO2在该反应中显__性。
(4)由图乙和图丙中的现象写出NO2和SO2反应的化学方程式:___。
Ⅱ.某课外活动小组欲探究镁与NO2的反应。已知镁与CO2的反应为2Mg+CO2![]() 2MgO+C。
2MgO+C。
(1)该小组类比Mg与CO2的反应对Mg与NO2的反应进行猜测,写出Mg与NO2反应的化学方程式:__。
(2)该小组设计如下实验验证上述猜测,实验装置(用于连接玻璃管的乳胶管均内衬锡纸)如图所示。
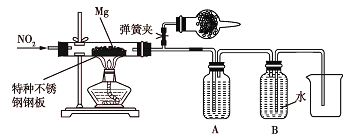
资料信息:2NO2+2NaOH=NaNO2+NaNO3+H2O
①装置A中的试剂是__。
②干燥管和装置B的作用分别是__、__。
③正确的实验操作步骤是__。
a.通人NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红棕色气体后,关闭弹簧夹
【答案】下 两气体混合后,红棕色消失 NO 氧化 NO2+SO2=NO+SO3 4Mg+2NO2![]() 4MgO+N2 NaOH溶液 吸收NO2避免污染环境 收集N2 badc
4MgO+N2 NaOH溶液 吸收NO2避免污染环境 收集N2 badc
【解析】
Ⅱ.该实验中先通入二氧化氮气体可排尽装置中的空气,此时打开弹簧夹,干燥管吸收多余的二氧化氮,然后关闭弹簧夹,之后点燃酒精灯,二氧化氮与镁单质发生反应,A装置中盛放氢氧化钠溶液可吸收为反应的二氧化氮,B装置短进长出且装满水,可用排水法收集反应生成的氮气。
I.(1)NO2呈红棕色,SO2为无色气体,故下瓶气体颜色深;
(2)NO2有强氧化性,能被SO2,还原成NO,则两气体混合后,红棕色消失;
(3)“有红棕色气体产生”说明SO2和NO2反应的产物中有NO,NO遇空气被氧化成NO2,SO2与NO2的反应中NO2体现了氧化性;
(4)NO2和SO2反应的化学方程式为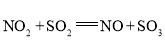 ;
;
Ⅱ.(1)由题意分析可知,Mg与NO2发生置换反应,反应的化学方程点燃式为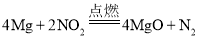 ;
;
(2)①由反应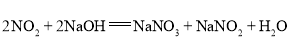 可知,装置A中的试剂是NaOH溶液,作用是除去N2中混有的NO2;
可知,装置A中的试剂是NaOH溶液,作用是除去N2中混有的NO2;
②干燥管的作用是吸收NO2避免污染环境。装置B是利用排水法收集N2的装置;
③正确的实验操作步骤是:打开弹簧夹→通入NO2(排尽装置中的空气)→当硬质玻璃管充满红棕色气体后,关闭弹簧夹,点燃酒精灯。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________ ,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③为__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体, 一定条件下发生如下反应:3A(g) ![]() B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是

A. 若t1=15s, A 的浓度变化表示 t0~t1阶段的平均反应速率为 0.09 mol·L-1·s-1
B. t0~t1阶段,此过程中容器放出a kJ热量,该反应的热化学方程式为:3A(g)![]() B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
C. 该容器的容积为2 L,B的起始的物质的量为0.03 mol
D. t1时该反应达到平衡且A 的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在400℃、101 kPa时,NO2(g) +CO(g) ![]() NO(g) + CO2(g) 反应过程的能量变化如下图所示。
NO(g) + CO2(g) 反应过程的能量变化如下图所示。
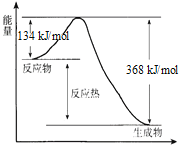
反应过程
(1)该反应是_____________(填“吸热”或“放热”)反应。
(2)该反应的热化学方程式为_____________。
(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是_____________。
a.浓度 b.压强 c.温度 d.催化剂
(4)反应体系中加入催化剂对反应热是否有影响?____(填“是”或“否”),原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KAl(SO4)2·12H2O]在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量SiO2和FeO·xFe2O3)可制备明矾。工艺流程如下:
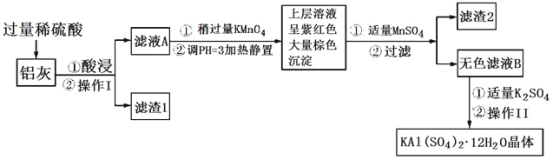
回答下列问题:
(1)明矾净水的原理是___(用离子方程式表示)。
(2)操作Ⅰ是___,操作Ⅱ是蒸发浓缩、___、过滤、___、干燥。
(3)检验滤液A中是否存在Fe2+的试剂是___(只用一种试剂)。
(4)在滤液A中加入高锰酸钾的作用:___。
(5)已知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:___,滤渣2含有的物质是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中进行着如下反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其平衡常数K和温度t的关系:
CO(g)+H2O(g),其平衡常数K和温度t的关系:
t℃ | 700 | 800 | 850 | 1000 | 1200 |
K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1)K的表达式为:_________;
(2)该反应的正反应为_________反应(“吸热”或“放热”);
(3)下列选项中可作为该反应在850℃时已经达到化学平衡状态的标志的是:_________。
A.容器中压强不再变化 B.混合气体中CO浓度不再变化
C.混合气体的密度不再变化 D.c(CO2)=c(CO)=c(H2)=c(H2O)
(4)当温度为850℃,某时刻测得该温度下的密闭容器中各物质的物质的量见表:
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
此时上述的反应中正、逆反应速率的关系式是_________(填代号)。
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.无法判断
(5)在700℃通过压缩体积增大气体压强,则该反应中H2(g)的转化率_________(“增大”、“减小”或“不变”);工业生产中,通过此方法使容器内气体压强增大以加快反应,却意外发现H2(g)的转化率也显著提高,请你从平衡原理解释其可能原因是__________________________________________。
Ⅱ.设在容积可变的密闭容器中充入10molN2(g)和10molH2(g),反应在一定条件下达到平衡时,NH3的体积分数为0.25。
(6)求该条件下反应N2(g)+3H2(g)![]() 2NH3(g)的平衡常数__________。(设该条件下,每1mol气体所占的体积为VL)上述反应的平衡时,再充入10mol的N2,根据计算,平衡应向什么方向移动?[需按格式写计算过程,否则答案对也不给分]__________。
2NH3(g)的平衡常数__________。(设该条件下,每1mol气体所占的体积为VL)上述反应的平衡时,再充入10mol的N2,根据计算,平衡应向什么方向移动?[需按格式写计算过程,否则答案对也不给分]__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法中正确的是
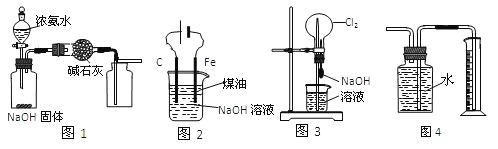
A. 用图1装置制取干燥纯净的NH3
B. 用图2装置制备Fe(OH)2并能较长时间观察其颜色
C. 用图3装置可以完成“喷泉”实验
D. 用图4装置测量Cu与浓硝酸反应产生气体的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种化合物,它们分别由下列五种原子团的两种不同的基团组成,这五种基团是-CH3,-C6H5,-OH,![]() ,
,![]() 。
。
已知:(1) A是无色晶体,有特殊气味,在空气中易氧化成粉红色;
(2) B、C能发生银镜反应,C的分子量大于B;
(3) D的水溶液与少量氢氧化钠溶液反应,生成-1价的阴离子;与过量氢氧化钠溶液反应,生成-2价阴离子。D可以和A的钠盐反应生成A;
(4) E可以由B氧化制取;
(5) F能氧化成饱和一元醛。
根据上述条件,推断其结构简式分别为:
A____________________B_____________________C_______________
D__________________E_____________________F________________。
上述A、D、E的酸性由强到弱的顺序是_____________________________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图.下列说法正确的是 ( )

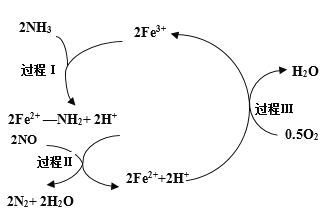
A.NH3催化还原NO为吸热反应
B.过程Ⅰ中NH3断裂非极性键
C.过程Ⅱ中NO为氧化剂,Fe2+为还原剂
D.脱硝的总反应为: 4NH3(g)+4NO(g)+ O2(g) ![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com