
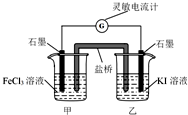
| A. | 反应开始时,乙中石墨电极上发生氧化反应 | |
| B. | 反应开始时,甲中石墨电极为正极 | |
| C. | 电流计读数为零时,反应达到化学平衡状态 | |
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |
分析 根据常温下能自动发生的氧化还原反应都可设计成原电池,再利用正反应2Fe3++2I-?2Fe2++I2可知,铁元素的化合价降低,而碘元素的化合价升高,则图中甲烧杯中的石墨作正极,乙烧杯中的石墨作负极,利用负极发生氧化反应,正极发生还原反应,并利用平衡移动来分析解答.
解答 解:A.因乙中I-失去电子放电,元素的化合价升高,则发生氧化反应,故A正确;
B.由总反应方程式知,Fe3+被还原成Fe2+,则发生还原反应,为正极,故B正确;
C.当电流计为零时,说明没有电子发生转移,则反应达到平衡,故C正确;
D.当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故D错误;
故选D.
点评 本题是对原电池原理综合考查,并注重与化学平衡的联系,学生明确原电池的工作原理、正负极的判断方法、化学平衡的移动即可解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ${Fe}_{2}{O}_{3}\stackrel{HCl(aq)}{→}{FeCl}_{3}(aq)\stackrel{△}{→}{Fe(OH)}_{3}(胶体)$ | |
| B. | ${Al}_{2}{O}_{3}\stackrel{NaOH(aq)}{→}{NaAlO}_{2}(aq)\stackrel{HCl(aq)}{→}{AlCl}_{3}$ | |
| C. | ${MgCl}_{2}(aq)\stackrel{石灰乳}{→}Mg{(OH)}_{2}\stackrel{煅烧}{→}MgO$ | |
| D. | $Fe{S}_{2}\stackrel{煅烧}{→}{SO}_{3}\stackrel{{H}_{2}O}{→}{H}_{2}{SO}_{4}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 镁粉和铝粉分别与等浓度、等体积的过量盐酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁粉和铝粉分别与等浓度、等体积的过量盐酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )| A. | 镁粉和铝粉的物质的量之比为3:2 | |
| B. | 镁粉和铝粉质量之比为3:2 | |
| C. | 镁粉和铝粉的摩尔质量之比为2:3 | |
| D. | 镁粉和铝粉反应完所需时间之比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种溶液pH的大小顺序是 ③>②>① | |
| B. | 若将3种溶液稀释相同倍数,pH变化最大的是② | |
| C. | 若分别加入25mL0.1mol•L-1盐酸后,pH最大的是① | |
| D. | 若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
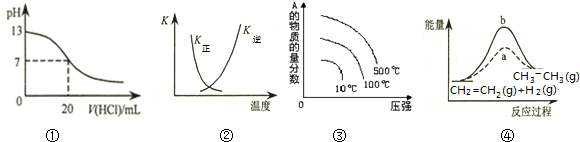
| A. | 图①表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)═2SO3(g)△H<0,正、逆反应的平衡常数K随温度的变化 | |
| C. | 对于可逆反应:A2(g)+3B2(g)?2AB3(g)△H>0,图③表示的是压强、温度、A的物质的量的分数的关系 | |
| D. | 图④中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g)△H<0,使用和未使用催化剂时,反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | NaClO溶液中通入少量SO2:3ClO-+SO2+H2O═Cl-+SO42-+2HClO | |
| C. | 向稀NH4HCO3溶液中加入过量NaOH溶液:NH4++OH-═NH3•H2O | |
| D. | 10 mL 0.5 mol•L-1的KAl(SO4)2溶液与20 mL 0.5 mol•L-1的Ba(OH)2溶液混合反应:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com