
| A. | 0.50 mol Ba(OH)2 | B. | 100 mL水 | C. | 0.50molC2H5OH | D. | 0.50molNa2SO4 |
分析 溶液导电性和离子浓度大小有关,
A.生成硫酸钡和水,溶液中离子浓度减小;
B.硫酸的浓度降低了,减弱;
C.酒精是不能导电,影响了硫酸的电离,减弱;
D.增加了电解质导电性增强.
解答 解:A.与H 2 SO 4 完全反应,生成硫酸钡沉淀溶液中离子浓度减小,溶液导电能力减弱,故A错误;
B.溶液的体积扩大,大约为原来的2倍,c(H+ )和c(SO42-),都变为原来的一半,溶液导电能力减弱,故B错误;
C.酒精是非电解质,溶解在水中,扩大了溶液的体积,降低了H+、SO42-的浓度,溶溶液导电能力减弱,故C错误;
D.Na2SO4与硫酸不反应,Na2SO4在溶液中完全电离成离子,增加了离子的总浓度,溶液的导电性增强,故D正确;
故选D.
点评 本题考查了溶液导电性的分析判断,注意反应混合后溶液中离子浓度的变化分析,掌握基础是关键,题目较简单.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
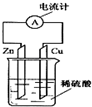 如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )
如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )| A. | 该装置将电能转变为化学能 | B. | 电流从锌片经导线流向铜片 | ||
| C. | 一段时间后,铜片质量减轻 | D. | 锌片上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 改变条件 | 平衡移动方向 | pH | 水电离出的c(H+) | KW |
| 升温 | ||||
| 通入HCl气体 | ||||
| 加入NaOH固体 | ||||
| 加入NH4Cl固体 | ||||
| 加入金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 假设 | 实验验证方法及现象 | |
| 假设1 | 白色浑浊物是BaSO3 | (1)在白色浑浊物中加入过量盐酸,会变澄清 |
假设2 | (2)白色浑浊物是BaSO4,主要 原因是Fe3+氧化了水中的SO2,在Ba2+作用下,生成BaSO4 | 反应开始前,先向制取SO2的装置中通入纯净的CO2,再把产生的SO2通入BaCl2溶液中,不出现浑浊.滴加FeCl3溶液后出现浑浊; (3)通入纯净的CO2的目的防止制备的SO2气体中混有空气(O2)对说明Fe3+氧化SO2造成干扰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 第二周期ⅣA族 第二周期ⅢA族 第七周期ⅣA族 | |
| B. | 第四周期ⅡA族 第二周期ⅢA族 第七周期ⅣA族 | |
| C. | 第二周期ⅣA族 第三周期ⅡA族 第四周期ⅦA族 | |
| D. | 第二周期ⅣA族 第三周期ⅡA族 第四周期ⅣA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 g氖气所含原子数为6.02×1023 | |
| B. | 25℃时,pH=6的水溶液中c(H+)>c(OH-) | |
| C. | 实验室制氢气时加入少量CuSO4可加快反应速率是利用了盐类的水解 | |
| D. | 把16.0 g无水硫酸铜粉末放在足量饱和硫酸铜溶液中会析出25.0 g晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.12mol/(L•min) | B. | 0.06mol/(L•min) | C. | 0.08mol/(L•h) | D. | 0.12mol/(L•h) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com