
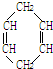
 可简写为
可简写为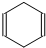 .现有某化合物W的分子结构可表示为
.现有某化合物W的分子结构可表示为 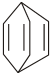 .
.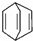 可写出分子式;
可写出分子式; 知,W的分子式为:C8H8,故答案为:C8H8;
知,W的分子式为:C8H8,故答案为:C8H8; 为是对称结构,该化合物中只有两类氢原子,所以其一氯代物有2种,故答案为:2;
为是对称结构,该化合物中只有两类氢原子,所以其一氯代物有2种,故答案为:2;

科目:高中化学 来源: 题型:
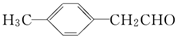 )转化为对甲基苯乙炔(
)转化为对甲基苯乙炔(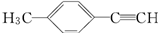 )的一条合成路线如下:
)的一条合成路线如下: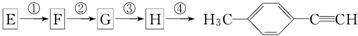 (G为相对分子质量为118的烃).
(G为相对分子质量为118的烃).| 序号 | 所加试剂及反应条件 | 反应类型 |
| ① | ||
| ② | ||
| ③ | ||
| ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/(min) | n(A)/( mol) | n(B)/( mol) | n(C)/( mol) |
| 0 | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.4 |
| 第4min | 0.4 | 1.8 | 1.2 |
| 第6min | 0.4 | 1.8 | 1.2 |
| 第8min | 0.1 | 2.0 | 1.8 |
| 第9min | 0.05 | 1.9 | 0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCN |
| 氢离子 |
| 水解 |


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取11.7g食盐 |
| B、用量筒量取12.36ml盐酸 |
| C、用酸式滴定管量取21.20ml 0.10mol/L H2SO4溶液 |
| D、用200ml容量瓶配制500ml 0.1mol/L NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、26.3% | B、73.7% |
| C、67.7% | D、95% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液面在“0”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛液体的体积 |
| B、相同温度下,0.2mol?L-1醋酸溶液和0.1mol?L-1醋酸溶液中的c(H+) |
| C、在0.1mol?L-1NaHSO4溶液中,阳离子数与阴离子数 |
| D、在FeCl2溶液中,c(Cl-)与c(Fe2+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com