
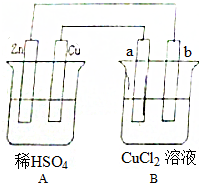
·ÖĪö ¢ŁA×°ÖĆĪŖŌµē³Ų£¬Zn±ČCu»īĘĆ×÷øŗ¼«£¬ŠæČܽā·¢ÉśŃõ»Æ·“Ó¦£¬Cu×÷Õż¼«CuÉĻĒāĄė×ӵƵē×ÓÉś³ÉĒāĘų·¢Éś»¹Ō·“Ó¦£»
¢ŚB×°ÖĆab¶¼ĪŖŹÆÄ«°ō¼“ĪŖµē½ā³Ų£¬ÓėCuĻąĮ¬µÄaĪŖŃō¼«ĀČĄė×ÓŹ§µē×ӷųöĀČĘų£¬ÓėZnĻąĮ¬µÄbĪŖŅõ¼«ĶĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£»
¢Ūøł¾Ż·ÖĪö¢Ł¢Ś½ā“š£»
¢Üøł¾ŻĆæŅ»øöµē¼«ÉĻµÄµĆŹ§µē×ÓŹżÄæĻąµČÅŠ¶Ļ£»
¢Żøł¾ŻČܽāµÄŠæµÄÖŹĮæ½įŗĻ×ŖŅʵē×ÓĻąµČ¼ĘĖć£®
½ā“š ½ā£ŗ¢ŁA×°ÖĆĪŖŌµē³Ų£¬Zn±ČCu»īĘĆ×÷øŗ¼«£¬ŠæČܽā·¢ÉśŃõ»Æ·“Ó¦£¬Cu×÷Õż¼«CuÉĻĒāĄė×ӵƵē×ÓÉś³ÉĒāĘų·¢Éś»¹Ō·“Ó¦£¬ĖłŅŌAÉձ֊擵½µÄĻÖĻóĪŖøŗ¼«Šæ²»¶ĻČܽā£¬Õż¼«Ķ±ķĆęÓŠĘųÅŻ²śÉś£¬¹Ź“š°øĪŖ£ŗøŗ¼«Šæ²»¶ĻČܽā£¬Õż¼«Ķ±ķĆęÓŠĘųÅŻ²śÉś£»
¢ŚB×°ÖĆab¶¼ĪŖŹÆÄ«°ō¼“ĪŖµē½ā³Ų£¬ÓėCuĻąĮ¬µÄaĪŖŃō¼«ĀČĄė×ÓŹ§µē×ӷųöĀČĘų£¬ÓėZnĻąĮ¬µÄbĪŖŅõ¼«ĶĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£¬ĖłŅŌBÉձ֊擵½µÄĻÖĻóĪŖa°ō“¦ÓŠ»ĘĀĢÉ«µÄĘųĢå²śÉś£¬b°ōÉĻÓŠŗģÉ«µÄĶĪö³ö£¬¹Ź“š°øĪŖ£ŗa°ō“¦ÓŠ»ĘĀĢÉ«µÄĘųĢå²śÉś£¬b°ōÉĻÓŠŗģÉ«µÄĶĪö³ö£»
¢ŪA×°ÖĆĪŖŌµē³Ų£¬Zn±ČCu»īĘĆ×÷øŗ¼«£¬Cu×÷Õż¼«£»B×°ÖĆab¶¼ĪŖŹÆÄ«°ō¼“ĪŖµē½ā³Ų£¬ÓėCuĻąĮ¬µÄaĪŖŃō¼«£¬ÓėZnĻąĮ¬µÄbĪŖŅõ¼«£¬¹Ź“š°øĪŖ£ŗøŗ£»Õż£»Ōµē³Ų£»Ńō£»Ņõ£»µē½ā³Ų£»
¢ÜŅņĪŖŠæµē¼«ŠæŹ§µē×ÓČܽā·“Ó¦Ź½Zn-2e-=Zn2+£»CuÉĻĒāĄė×ӵƵē×ÓÉś³ÉĒāĘų·“Ó¦Ź½2H++2e-=H2”ü£»aĪŖŃō¼«ĀČĄė×ÓŹ§µē×ӷųöĀČĘų·“Ó¦Ź½ĪŖ2Cl--2e-=C12”ü£»bĪŖŅõ¼«ĶĄė×ӵƵē×ÓÉś³ÉĶ·“Ó¦Ź½ĪŖCu2++2e-=Cu£»ÓÖĆæŅ»øöµē¼«ÉĻµÄµĆŹ§µē×ÓŹżÄæĻąµČ£¬ĖłŅŌZn°ō”¢Cu°ō”¢a°ō”¢b°ōÉĻ·“Ó¦»ņÉś³ÉµÄĪļÖŹµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£ŗ1£ŗ1£¬“š£ŗŅ»¶ĪŹ±¼äŗóZn°ō”¢Cu°ō”¢a°ō”¢b°ōÉĻ·“Ó¦»ņÉś³ÉµÄĪļÖŹµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£ŗ1£ŗ1£»
¢ŻA×°ÖĆÖŠZn°ōÖŹĮæ¼õÉŁ3.25g£¬·“Ó¦Ź½Zn-2e-=Zn2+£¬¼“×ŖŅʵĵē×ÓĪŖ$\frac{3.25}{65}$”Į2=0.1mol£¬ÓÖŃō¼«ÉĻµÄµē¼«·“Ó¦ĪŖ£ŗ2Cl--2e-=Cl2”ü£¬ĖłŅŌĻūŗĵÄn£ØCl-£©=0.1mol£¬Ōņ“ĖŹ±BÖŠCl-µÄÅضČĪŖ$\frac{2”Į0.1”Į2-0.1}{0.1}$=3mol/L£»
“š£ŗ“ĖŹ±BÖŠCl-µÄÅضČĪŖ3mol/L£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌµē³ŲŌĄķŗĶµē½ā³ŲŌĄķµÄÓ¦ÓĆ£¬Ć÷Č·ÓŠ¹ŲŌĄķ¼°µē¼«·“Ó¦ŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢ÖŲ»ł“”ÖŖŹ¶µÄ漲飮


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NF3 | B£® | CH${\;}_{3}^{-}$ | C£® | SO3 | D£® | H3O+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬CO2
£¬CO2 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | A£¾B£¾D£¾C | B£® | B£¾D£¾A£¾C | C£® | D£¾A£¾B£¾C | D£® | D£¾B£¾A£¾C |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ėĀŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£®Ä³Ģ½¾æŠ”×éĄūÓĆĻĀĮŠ·“Ó¦ÖĘČ”Ė®ŗĻėĀ£ØN2H4•H2O£©£®CO£ØNH2£©+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
ėĀŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£®Ä³Ģ½¾æŠ”×éĄūÓĆĻĀĮŠ·“Ó¦ÖĘČ”Ė®ŗĻėĀ£ØN2H4•H2O£©£®CO£ØNH2£©+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ć¾ŹĒµŚIIA×åŌŖĖŲ | |
| B£® | µŚIA×åŌŖĖŲČ«²æŹĒ½šŹōŌŖĖŲ | |
| C£® | Ńõ×åÖŠŗ¬½šŹōŌŖĖŲ | |
| D£® | µŚ3ÖÜĘŚÖŠ¼ČÓŠ½šŹōŌŖĖŲÓÖÓŠ·Ē½šŹōŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
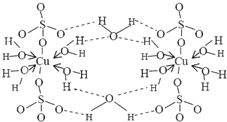 ²Ø¶ū¶ąŅŗŹĒŅ»ÖÖ±£»¤ŠŌɱ¾ś¼Į£¬¹ć·ŗÓ¦ÓĆÓŚŹ÷ľ”¢¹ūŹ÷ŗĶ»Ø»ÜÉĻ£¬ĻŹĄ¶É«µÄµØ·Æ¾§ĢåŹĒÅäÖĘ²Ø¶ū¶ąŅŗµÄÖ÷ŅŖŌĮĻ£®µØ·ÆCuSO4?5H2OæÉŠ“³É[Cu£ØH2O£©4]SO4?H2O£¬Ęä½į¹¹Ź¾ŅāĶ¼ČēĶ¼£ŗ
²Ø¶ū¶ąŅŗŹĒŅ»ÖÖ±£»¤ŠŌɱ¾ś¼Į£¬¹ć·ŗÓ¦ÓĆÓŚŹ÷ľ”¢¹ūŹ÷ŗĶ»Ø»ÜÉĻ£¬ĻŹĄ¶É«µÄµØ·Æ¾§ĢåŹĒÅäÖĘ²Ø¶ū¶ąŅŗµÄÖ÷ŅŖŌĮĻ£®µØ·ÆCuSO4?5H2OæÉŠ“³É[Cu£ØH2O£©4]SO4?H2O£¬Ęä½į¹¹Ź¾ŅāĶ¼ČēĶ¼£ŗ £¬ÓėĶĶ¬ÖÜĘŚµÄĖłÓŠŌŖĖŲµÄ»łĢ¬Ō×ÓÖŠ×īĶā²ćµē×ÓŹżÓėĶŌ×ÓĻąĶ¬µÄŌŖĖŲÓŠK”¢Cr£ØĢīŌŖĖŲ·ūŗÅ£©£®
£¬ÓėĶĶ¬ÖÜĘŚµÄĖłÓŠŌŖĖŲµÄ»łĢ¬Ō×ÓÖŠ×īĶā²ćµē×ÓŹżÓėĶŌ×ÓĻąĶ¬µÄŌŖĖŲÓŠK”¢Cr£ØĢīŌŖĖŲ·ūŗÅ£©£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com