
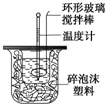
 利用下图装置测定中和热的实验步骤如下:
利用下图装置测定中和热的实验步骤如下:| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
分析 (1)中和热是强酸和强碱的稀溶液完全反应生成1mol水放出的热量,根据热化学方程式的书写方法写出热化学方程式;
(2)将NaOH溶液倒入小烧杯中,不能分几次倒入,否则会导致热量散失,影响测定结果;
(3)硫酸和氢氧化钠混合时,用套在温度计上的环形玻璃搅拌棒轻轻地搅动,使硫酸与NaOH溶液混合均匀;
(4)①先判断温度差的有效性,然后求出温度差平均值;
②根据Q=m•c•△T计算反应放出的热量,最后根据△H=-$\frac{Q}{n}$kJ/mol计算出反应热.
解答 解:(1)强酸、强碱的中和热为-57.3kJ/mol,中和热是强酸和强碱的稀溶液完全反应生成1mol水放出的热量,稀硫酸和稀氢氧化钠溶液反应的热化学方程式为:$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol;
故答案为:$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol;
(2)倒入氢氧化钠溶液时,必须一次迅速的倒入,目的是减少热量的散失,不能分几次倒入氢氧化钠溶液,否则会导致热量散失,影响测定结果,
故选:C;
(3)使硫酸与NaOH溶液混合均匀的正确操作方法是:用套在温度计上的环形玻璃搅拌棒轻轻地搅动;温度计是测量温度的,不能使用温度计搅拌;也不能轻轻地振荡烧杯,否则可能导致液体溅出或热量散失,影响测定结果;更不能打开硬纸片用玻璃棒搅拌,否则会有热量散失;
故选:D;
(4)①4次温度差分别为:3.4℃,5.1℃,3.3℃,3.5℃,第2组数据无效,温度差平均值为3.4℃;
故答案为:3.4℃;
②50mL 0.5mol/L盐酸与50mL 0.55mol/L NaOH溶液进行中和反应生成水的物质的量为0.05L×0.5mol/L=0.025mol,溶液的质量为100ml×1g/cm3=100g,温度变化的值△T=3.4℃,则生成0.025mol水放出的热量为Q=m•c•△T=100g×4.18J/(g•℃)×3.4℃=1421.2J,即1.4212kJ,所以实验测得的中和热△H=-$\frac{1.4212kJ}{0.025mol}$=-56.8kJ/mol;
故答案为:-56.8kJ/mol.
点评 本题考查了中和热的测定方法,题目难度不大,注意掌握测定中和热的正确方法,明确实验操作过程中关键在于尽可能减少热量散失,使测定结果更加准确.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子序数116 | B. | 中子数177 | C. | 核外电子数116 | D. | 相对原子质量293 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为9NA | |
| B. | 1mol/L的Mg(NO3)2溶液中含有的NO3-的数目为2 NA | |
| C. | 铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA | |
| D. | 42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖、硫酸钡和水分别属于非电解质、强电解质、弱电解质 | |
| B. | 甲醇、乙二醇(HOCH2CH2OH)互为同系物 | |
| C. | 除去CO2中混有的SO2:用饱和NaHCO3溶液洗气,再干燥 | |
| D. | 液溴易挥发,盛放在用水密封、玻璃塞塞紧的棕色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )
如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )| A. | N点时溶液中的溶质只有NaCl | |
| B. | c(NaOH)=c(HCl) | |
| C. | 原混合溶液中c(MgCl2):c(AlCl3)=1:2 | |
| D. | K点之前加入的是NaOH溶液,K点之后加入的是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业可采用火法炼铜:Cu2S+O2═2Cu+SO2 每生成2mol铜,反应共转移6NA个电子 | |
| B. | 标准状况下,11.2L甲苯含有的分子数为0.5NA | |
| C. | 20g重水(D2O)所含的电子数为10NA | |
| D. | 60gSiO2中共用电子对数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1=V2>V3 | B. | V1=V2=V3 | C. | V3>V2>V1 | D. | V3>V2=V1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 阳离子 | 阴离子 |
| Na+ Ca2+ Fe 2+ Al3+ Fe 3+ Mg3+ | OH- HCO3- CO32- Cl- NO3- SO42- |
| A. | X溶液中不可能含有HCO3-或CO32- | |
| B. | 生成无色气体的离子方程式为:3Fe2++NO3-+4H+═3Fe3++NO+2H2O | |
| C. | 根据电荷守恒,原溶液中一定含Mg2+ | |
| D. | X溶液中一定含3种阳离子、2种阴离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com