
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是
A. 常温下,1mol—OH所含的电子数目为9NA
B. 常温下,在16g 18O2中含有NA个氧原子
C. 1 mol乙烷中含有C—H的键数为7NA
D. 标准状况下,11.2LSO2与足量O2反应生成SO3分子数 0.5NA
【答案】A
【解析】本题考查有关阿伏伽德罗常数的计算。根据—OH的结构确定电子数目;根据物质的量公式确定氧原子数;根据乙烷的结构确定C-H键数;根据SO2与足量O2反应生成SO3是可逆反应,确定生成SO3的微粒数。
A、常温下,—OH所含的电子数目为9个电子,所以1mol—OH所含的电子总数为9NA,故A正确;B.常温下,在16g 18O2中含有的氧原子数为16g/36(g.mol-1)![]() 2=0.89NA,故B错误;C. 乙烷的结构简式为CH3CH3,含有6个C—H共价键和1个C-C共价键,1 mol乙烷中含有C—H的键数为6NA,故C错误;D.因为SO2与O2反应为可逆的,所以标准状况下,11.2LSO2与足量O2反应生成SO3分子数小于 0.5NA,故D错误;答案选A。
2=0.89NA,故B错误;C. 乙烷的结构简式为CH3CH3,含有6个C—H共价键和1个C-C共价键,1 mol乙烷中含有C—H的键数为6NA,故C错误;D.因为SO2与O2反应为可逆的,所以标准状况下,11.2LSO2与足量O2反应生成SO3分子数小于 0.5NA,故D错误;答案选A。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】下图是一种已投入生产的大型蓄电系统。电解质通过泵不断地在储罐和电池间循环;中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为Na2S4和NaBr。下列说法正确的是

A. 左储罐中的电解质为Na2S2,右储罐中的电解质为NaBr3
B. 在充电过程中钠离子通过膜的流向为从右到左
C. 放电时,正极的电极反应为Na2S4+2Na++2e-=2Na2S2
D. 电池充电时,阳极的电极反应为3NaBr-2e-= NaBr3 + 2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中不正确的是( )
A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3﹣O﹣CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:苯和卤代烃在催化剂的作用下可以生成烷基苯和卤化氢,C是生活中常见的有机物,75%的C溶液可用于医用消毒,乙苯能被酸性高锰酸钾溶液氧化为苯甲酸.几种物质之间的转化关系如图所示(生成物中所有无机物均已略去).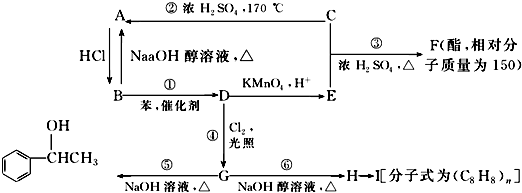
请回答下列问题:
(1)写出物质的结构简式:D;I .
(2)在①~⑥6个反应中,属于消去反应的是(填编号).
(3)写出下列反应的化学方程式:
①;
⑤;
(4)写出一种符合下列要求的F的同分异构体的结构简式:F的同分异构体中属于酯类,能发生银镜反应,且苯环上的一氯取代物只有两种: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.过量铁片与100mL 0.01mol/L的稀盐酸反应,能量变化趋势,如图所示:

(1)该反应为__________反应(填“吸热”或“放热”)。
(2)为了加快产生H2的速率而不改变H2的产量,可以使用如下方法中的______
①加H2O ②加入几滴1mol/LHNO3溶液 ③滴入几滴浓盐酸
④加入一定量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液
⑦适当升高温度(不考虑盐酸挥发) ⑧改用10mL0.1mol/L盐酸
A. ②③⑥⑦⑧ B. ③④7⑧ C. ③⑥⑦⑧ D. ③⑥⑦
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜电极上发生的电极反应为________。
Ⅱ.某温度时,在5 L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:

(1)分析有关数据,写出X、Y、Z的反应方程式__________。
(2)该反应在3种不同条件下进行,其中Y起始浓度相同,Z起始浓度为0,反应物X的浓度随反应时间的变化情况如下表:

①实验1中,在10~20min内,以物质Y表示的平均反应速率为________mol/(L·min) ,50min时,实验3中Z的浓度________。
②0~20min内,其它条件一样实验2和实验1的反应速率不同,其原因可能是__________;实验3和实验1的反应速率不同,其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用乙醇与浓硫酸来制取乙烯,反应装置如下图A所示,发生反应为CH3CH2OH ![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O

请回答下列问题:
Ⅰ.制取实验中,混合乙醇与浓硫酸的操作是_________,通常在圆底烧瓶中加入几粒碎瓷片的作用是_________________,装置A图中一处明显的错误是____________________。
Ⅱ.用该方法在实验室制取乙烯时,常会看到烧瓶中液体变黑,并使装置A中制得的乙烯中混有CO2、SO2等杂质气体。为确定乙烯及各种杂质气体的存在,请用上面给出的实验装置完成下面的实验探究设计。
探究设计1:若要检验A中所得气体含有SO2,可将混合气体直接通入__________(填装置代号,下同)装置;若要检验A中所得气体含有乙烯,可将混合气体直接通入____________________。
探究设计2:若将A中所得气体依次通过①→②→③→E装置,根据实验现象可确定乙烯气体中混有二氧化硫气体。
则:(1)设计2中①→②→③装置对应的装置分别是___________________(填装置代号)。
(2)设计2中能说明二氧化硫气体存在的现象是___________________________。
(3)使用装置②的目的是____________________。使用装置③的目的是________________________。
(4)设计2中确认乙烯气体存在的现象是_____________________。
探究设计3:若要一次性将乙烯、CO2、SO2三种气体全部检验出来,气体被检验出来的先后顺序是___________________,气体通过装置的顺序为A→______(填装置代号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com