
��֪298Kʱ��2SO2��g����O2��g��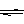 2SO3��g������H����197KJ��mol������ͬ���¶Ⱥ�ѹǿ�£����ܱ�������ͨ��2molSO2��1molO2���ﵽƽ��ʱ�ų�����Q1������һ�������ͬ��������ͨ��1molSO2��0��5molO2��1molSO3���ﵽƽ��ʱ�ų�����Q2�������й�ϵʽ��ȷ���ǣ� ��
2SO3��g������H����197KJ��mol������ͬ���¶Ⱥ�ѹǿ�£����ܱ�������ͨ��2molSO2��1molO2���ﵽƽ��ʱ�ų�����Q1������һ�������ͬ��������ͨ��1molSO2��0��5molO2��1molSO3���ﵽƽ��ʱ�ų�����Q2�������й�ϵʽ��ȷ���ǣ� ��
| A��Q1��Q2��197KJ | B��Q1��Q2��197KJ | C��Q2��Q1��197KJ | D��Q1��Q2��197KJ |
C
��������������ɷ�Ӧ����ʽ�п��Կ�����ÿ��2mol��SO2������Ӧ�ų�����Ϊ197KJ.�����ڸ÷�Ӧ�ǿ��淴Ӧ�������ܱ�������ͨ��2molSO2��1molO2ʱ�����ܷ�Ӧ��ȫ�����Էų�����ҪС��197KJ.������һ�������ͬ��������ͨ��1molSO2��0��5molO2��1molSO3�����൱��ֻ����1molSO2��0��5molO2�����ڼ�С��Ӧ��Ũ�ȣ���ѧƽ�������ƶ������ȱȵ�һ��������١����Թ�ϵʽ��ȷ����Q2��Q1��197KJ ��ѡ��Ϊ��C��
���㣺������淴Ӧ���ص㼰��Ӧ�ȵ��йؼ����֪ʶ��


 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ס��ҡ��������ܱ������зֱ����һ������A��B��������Ӧ��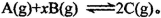 ���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ�����ͼ����ʾ��
���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ�����ͼ����ʾ��
����˵����ȷ����
A��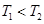 ���Ҹ÷�ӦΪ���ȷ�Ӧ
���Ҹ÷�ӦΪ���ȷ�Ӧ
B��x=2
C����ƽ����¶Ȳ��䣬�ı��������ƽ�ⲻ�ƶ�
D��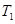 ���£�����ʼʱ��������г���0.5molA��1.5molB��ƽ��ʱA��ת����Ϊ25%
���£�����ʼʱ��������г���0.5molA��1.5molB��ƽ��ʱA��ת����Ϊ25%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����ݻ�Ϊ1 L�ļ����������º����ܱ�����������м���2 mol A�����2 mol B����������·�Ӧ��A(g)��B(g) C(g) ��H=" -a" kJ·mol-1����Ӧ�ﵽƽ��״̬ʱ����1 mol C���壬�ų�����Q1kJ�����м���1molC���壬��Ӧ�ﵽƽ��ʱ����������Q2kJ����Q1 ��Q2�����ϵ��ȷ���ǣ� ��
C(g) ��H=" -a" kJ·mol-1����Ӧ�ﵽƽ��״̬ʱ����1 mol C���壬�ų�����Q1kJ�����м���1molC���壬��Ӧ�ﵽƽ��ʱ����������Q2kJ����Q1 ��Q2�����ϵ��ȷ���ǣ� ��
| A��Q1 + Q2 = a | B��Q1 + 2Q2 < 2a | C��Q1 + 2Q2 > 2a | D��Q1 + Q2 < a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ�����İ�������粒��������ݻ��㶨����������У�������Ӧ��H2NCOONH4(s)  2NH3(g)��CO2(g)���ڲ�ͬ�¶��£��÷�Ӧ��ƽ��״̬ʱ�IJ������������ʾ������˵����ȷ����(����)
2NH3(g)��CO2(g)���ڲ�ͬ�¶��£��÷�Ӧ��ƽ��״̬ʱ�IJ������������ʾ������˵����ȷ����(����)
| �¶� | ƽ��Ũ��(mol·L��1) | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | | 0.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������£���NO2��SO2��2��3������������ܱ������з����Ϸ�Ӧ��NO2(g)+SO2(g) SO3(g)+NO(g)�����������Ӧƽ��ʱNO2��SO2�����Ϊ1��4����ƽ��ʱSO2(g)��ת�����ǣ� ��
SO3(g)+NO(g)�����������Ӧƽ��ʱNO2��SO2�����Ϊ1��4����ƽ��ʱSO2(g)��ת�����ǣ� ��
| A��5/6 | B��3/4 | C��5/9 | D��2/3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ʵ����Ҫ������ȡ��������õķ�����
| A����п��ϡ���ᷴӦ | B����п��Ũ���ᷴӦ |
| C����п��Ũ���ᷴӦ | D����п��ϡ���ᷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��Ӧ2CO(g)===2C(s)��O2(g)�Ħ�HΪ��ֵ����SΪ��ֵ���覤H�ͦ�S�����¶ȶ��䣬����˵����ȷ����
| A�����������Է����� |
| B�����������Է����� |
| C�������²����Է����У����������Է����� |
| D���κ��¶��¶������Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪ij���淴Ӧ��mA(g)+nB(g)  pC(g) ��H=Q kJ��mol-1�����ܱ������н��У���ͼ��ʾ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�İٷֺ����Ĺ�ϵ���ߣ������ж���ȷ����
pC(g) ��H=Q kJ��mol-1�����ܱ������н��У���ͼ��ʾ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�İٷֺ����Ĺ�ϵ���ߣ������ж���ȷ����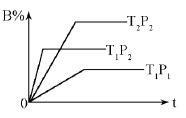
| A��T2��T1P1�� P2 m+n �� p �� ����0 |
| B��T1��T2P1�� P2 m+n �� p �� ����0 |
| C��T1��T2P1�� P2 m+n �� p �� ����0 |
| D��T1 ��T2P1�� P2 m+n �� p �� ����0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ж�һ����ѧ��Ӧ���Է��Գ������оݺ����оݣ�������������£������ж���Ӧһ���Է����е��ǣ� ��
| A����H>0����S>0 | B����H<0����S<0 |
| C����H>0����S<0 | D����H<0����S>0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com