
NaCl晶体模型如图所示,在NaCl晶NaCl的晶体结构体中,每个Na+周围同时吸引________个Cl-,每个Cl-周围也同时吸引着________个Na+;在NaCl晶胞中含有________个Na+、________个Cl-,晶体中每个Na+周围与它距离最近且相等的Na+共有________个。

解析 在氯化钠晶体中,一个Na+位于晶胞的中心,12个Na+分别位于晶胞的12条棱上,则属于该晶胞的Na+相当于3个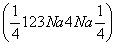 ,因此一个晶胞中共含有4个Na+;8个Cl-分别位于晶胞的8个顶点上,则属于该晶胞的Cl-相当于1个
,因此一个晶胞中共含有4个Na+;8个Cl-分别位于晶胞的8个顶点上,则属于该晶胞的Cl-相当于1个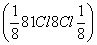 ,6个Cl-分别位于晶胞的6个面心上,则属于该晶胞的Cl-相当于3个
,6个Cl-分别位于晶胞的6个面心上,则属于该晶胞的Cl-相当于3个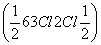 ,所以一个晶胞中共含有4个Cl-。可见NaCl晶体中Na+、Cl-的个数比为1∶1。图中位于晶胞中心的Na+实际上共有3个平面通过它,通过中心Na+的每个平面都有4个Na+位于平面的四角,这4个Na+与中心Na+距离最近且距离相等。所以在NaCl晶体中,每个Na+周围与它距离最近且距离相等的Na+共有12个,按相似的方法可推出每个Cl-周围与它距离最近且距离相等的Cl-也共有12个。
,所以一个晶胞中共含有4个Cl-。可见NaCl晶体中Na+、Cl-的个数比为1∶1。图中位于晶胞中心的Na+实际上共有3个平面通过它,通过中心Na+的每个平面都有4个Na+位于平面的四角,这4个Na+与中心Na+距离最近且距离相等。所以在NaCl晶体中,每个Na+周围与它距离最近且距离相等的Na+共有12个,按相似的方法可推出每个Cl-周围与它距离最近且距离相等的Cl-也共有12个。
答案 6 6 4 4 12


科目:高中化学 来源: 题型:
已知A(g) 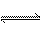 B(g)+C(g)反应的平衡常数和温度的关系如下:
B(g)+C(g)反应的平衡常数和温度的关系如下:
| 温度/ ℃ | 700 | 800 | 900 | 1000 |
| 平衡常数 | 0.4 | 0.9 | 1.0 | 1.6 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0,△S 0(填“<”“ >”“ =”)
(2)900℃时,向一个0.5 L的密闭容器中充入6mol的A,如反应初始5s内A的平均反应速率v(A)=0.4 mol·L-1·s-1。则5s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 。保持温度和体积不变,再向容器中充入4mol的A,则重新达到平衡时A的转化率为
(3)700℃时反应C(g)+B(g) A(g)的平衡常数的值为
A(g)的平衡常数的值为
查看答案和解析>>
科目:高中化学 来源: 题型:
在A、B两支大试管中分别依次加入苯、H2O,再用长颈漏斗小心加入CCl4。两试管中都明显分为三层,将A试管振荡后静置(已知苯的密度小于水的密度而四氯化碳的密度大于水的密度)。
(1)溶液可分为________层,原因是________________________________。
(2)不用实验验证你能否判断出哪一层是水层_________,若能,判断的依据是________________________________________________________________________
(若不能,此问可不回答)。
(3)请你设计简单实验验证哪一层是水层: _________________________________
________________________________________________________________________。
(4)用长颈漏斗向B试管中的水层小心加入少量浓溴水,静置一段时间,试管中的现象是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。请填写下列空白:
【实验一】用如图CB31所示装置,收集一量筒甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
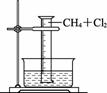
图CB31
(1)该反应的反应类型为______________。
(2)该反应的化学方程式为____________________________________________________
(只写第一步)。
(3)水槽中盛放的液体应为________(填标号)。
A.水 B.饱和石灰水 C.饱和食盐水 D.饱和NaHCO3溶液
【实验二】收集一试管甲烷和氯气的混合气体,光照反应后,滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成。
(4)该实验设计的错误之处是_________________________________________________。
【实验三】步骤一:收集半试管氯气,加入10 mL蒸馏水,充分振荡,采用DIS系统的pH传感器测量溶液的pH(下同),测得pH=3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,加入10 mL蒸馏水,充分振荡,测得pH=1.00。
(5)判断该反应中有氯化氢生成的依据是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是 ( )。
A.非金属元素的两原子之间不可能形成离子键
B.离子化合物不可能全部由非金属元素组成
C.含有非极性键的分子不一定是共价化合物
D.离子化合物中一定含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素,Y原子基态时最外层电子数是其内层电子总数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为________,1 mol Y2X2含有σ键的数目为________。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是________。
 (3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是________。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是________。
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯
化物的化学式是________,它可与浓盐酸发生非氧化还
原反应,生成配合物HnWCl3,反应的化学方程式为
_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强,如下表所示:
含氧酸酸性强弱与羟基氧原子数的关系
|
(1)亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性差别很大,
H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构
简式分别为① ,② 。
(2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
① ,② 。
(3)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况: ,
写出化学方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第ⅠB族。Cu2+的核外电子排布式为 。
(2)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知
NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原
因是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
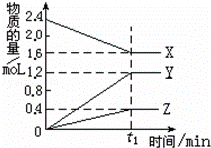
某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:
(1)①该反应的化学方程式.
②在t1min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为2:3
C.生成3mol Y的同时生成1mol Z
D.生成1mol Z的同时生成2mol X
(2)①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则至t1min时,该反应吸收的热量为:;在此t1min时间内,用H2表示反应的平均速率v(H2)=.
②两位同学讨论放热反应和吸热反应.甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应.你认为他们说法正确的是同学.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com