


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 W、X、Y、Z为原子序数依次增大的前四周期元素,其中W、X、Y为主族元素.用X的氧化物漂白的草帽日久又变成黄色;基态W原子有两个单电子,且与X不同周期不同族,X、Y同周期,基态Z原子电子分属7个能级,且各能级均为全充满.
W、X、Y、Z为原子序数依次增大的前四周期元素,其中W、X、Y为主族元素.用X的氧化物漂白的草帽日久又变成黄色;基态W原子有两个单电子,且与X不同周期不同族,X、Y同周期,基态Z原子电子分属7个能级,且各能级均为全充满.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
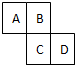 如图为元素周期表的一部分,已知A、B、C、D均为短周期元素,A与D原子序数之和是C的原子序数的1.5倍.
如图为元素周期表的一部分,已知A、B、C、D均为短周期元素,A与D原子序数之和是C的原子序数的1.5倍.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应前2min的平均速率v(SO2)=0.1amol/(L.min) |
| B、当混合气体的物质的量不再改变时,反应达到平衡状态 |
| C、平衡后保持其它条件不变,从容器中分离出部分硫,平衡向正反应方向移动 |
| D、平衡后保持其他条件不变,升高温度和加入催化剂,SO2的转化率均增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com