
 CF4
CF4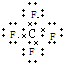 BaCl2
BaCl2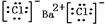 N2
N2 CO2
CO2 .
. 分析 氢氧化钾为离子化合物,电子式需要标出阴阳离子所带电荷;CF4是共价化合物,各原子满足稳定结构;BaCl2为离子化合物,由1个钡离子和2个氯离子构成;
氮气为单质,N原子之间为氮氮三键;二氧化碳为共价化合物,C原子和两个O原子间均为双键.
解答 解:氢氧化钾为离子化合物,由钾离子和氢氧根离子构成,氢氧化钾的电子式为: ;
;
CF4为共价化合物,各原子满足8电子稳定结构,电子式为 ;
;
BaCl2为离子化合物,由1个钡离子和2个氯离子构成,相同离子不能合并,故电子式为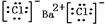 ;
;
氮气为单质,N原子之间为共价键且为氮氮三键,故电子式为: ;
;
二氧化碳为共价化合物,C原子和两个O原子间均为双键,故二氧化碳的电子式为 .
.
故答案为: ;
; ;
;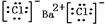 ;
; ;
; .
.
点评 本题考查了电子式的书写,题目难度不大,注意掌握电子式的正确表示方法,在书写电子式之前先判断物质的种类.


科目:高中化学 来源: 题型:解答题
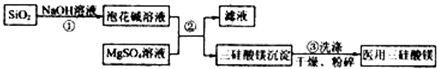
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ Cl- Mg2+ SO42- | B. | K+ Cu2+ I- SO42- | ||
| C. | NO3- K+ Cl- OH- | D. | Al3+ Na+ S2- Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2Cl2不存在同分异构体是甲烷正四面体结构的理由之一 | |
| B. |  和 和 互为同系物 互为同系物 | |
| C. | 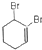 的系统命名的名称是1,2-二溴-2-环己烯 的系统命名的名称是1,2-二溴-2-环己烯 | |
| D. |  的名称为2-甲基-3-乙基丁烷 的名称为2-甲基-3-乙基丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
| 用该装置排空气法收集H2、CO2、Cl2等气体 | 蒸干AlCl3饱和溶液制备AlCl3晶体 | 可以证明氧化性Cl2>Br2>I2 | 比较不同催化剂对反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com