
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源:不详 题型:单选题
| A.两者都易溶于水 |
| B.两者都是有毒气体 |
| C.两者都能使品红溶液褪色 |
| D.两者都是形成酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2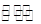 N2O4的 N2O4的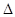 H<0 H<0 |
| B | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡 | 下层分别呈无色 和紫红色 | 还原性:I->Br->Fe2+ |
| C | 某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水 | 有白色沉淀出现 | 该钾盐是K2CO3 |
| D | 把SO2通入紫色石蕊试液中 | 紫色褪去 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2013年0点钟声敲响后的几个小时,北京的污染指数从轻度污染上升为重度污染,主要污染为PM2.5污染,看来烟花爆竹的燃放,可加重PM2.5污染 |
| B.催化剂之所以能加快反应速率,是因为催化剂能降低反应的活化能 |
| C.氨气的水溶液氨水可以导电,因此氨气是电解质 |
| D.大量燃烧含硫燃料是形成酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
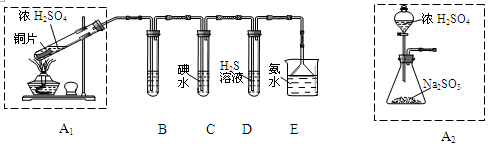
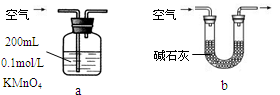
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,将反应后的混合气体先通过置于冰水浴的U型管,再通入足量的BaCl2溶液,结果为
N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,将反应后的混合气体先通过置于冰水浴的U型管,再通入足量的BaCl2溶液,结果为 | A.产生BaSO4和BaSO3沉淀 | B.无沉淀产生 |
| C.产生BaSO4沉淀 | D.产生BaSO3沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
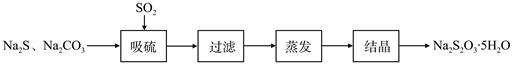
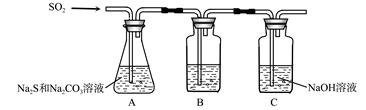
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,___________________。 | _______________ | 样品含NaCl |
| ② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,___________________。 | _______________ | 样品含NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.酸性 | B.吸水性 | C.脱水性 | D.强氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硝酸和浓硫酸露置于空气中,容器内酸液的浓度都降低 |
| B.可用铁制容器储存稀硝酸 |
| C.SO2溶于水生成H2SO4 |
| D.SO2通入BaCl2溶液中能产生白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com