
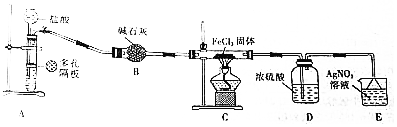
分析 氯化铁晶体(FeCl3•6H2O)制备少量氯化亚铁,流程为:由装置A制备氢气,制得的氢气含有氯化氢杂质和水,用B装置中的碱石灰吸收氯化氢和水蒸气,氢气与氯化铁在C处发生反应生成氯化亚铁和氯化氢气体,在E装置中氯化氢与硝酸银反应生成白色沉淀,因为氯化铁受遇水剧烈水解,故在C与E中加D装置浓硫酸吸收水蒸气,据此分析;
解答 解:(1)FeCl3•6H2O晶体得到无水氯化铁,应防止氯化铁水,需要在在HCl气流中加热蒸干;
故答案为:在HCl气流中加热蒸干;
(2)装置A中用Zn与稀盐酸制取氯气,发生的离子方程式为:Zn+2H+=Zn2++H2↑;
故答案为:Zn+2H+=Zn2++H2↑;
(3)反应中有气体参与,故装药品之前必须进行的操作是检验装置气密性;亚铁离子易被氧化,故实验时先打开A中活塞,过一会儿,用氢气排尽装置内的空气,再点燃C处酒精灯;
故答案为:检验装置气密性;用氢气排尽装置内的空气;
(4)C处为氯化铁与氢气反应生成氯化亚铁和氯化氢的反应,化学方程式为:2FeCl3+H2=FeCl2+HCl,氯化亚铁呈绿至黄色,故C中已发生反应的现象是有呈绿至黄色物质出现;
故答案为:有呈绿至黄色物质出现;2FeCl3+H2=FeCl2+HCl;
(5)样品中可能含有没反应完的氯化铁,能使KSCN显红色,不能确定是亚铁离子被双氧水氧化后的铁离子所致,故实验Ⅰ不能达到实验目的;氯化亚铁与重铬酸钾反应:6FeCl2+K2Cr2O7+14HCl=6FeCl3+2CrCl3+2KCl+7H2O,由于重铬酸钾橙红色,氯化亚铁为呈绿至黄色,而生成物FeCl3为橘黄色,CrCl3为深绿色,所以反应前后颜色不会变化太大,实验Ⅱ不能达到实验目的;
故答案为:样品中可能含有氯化铁;颜色变化不大,不易观察.
点评 本题考查了物质的制备,涉及离子方程式的书写,实验操作的控制,离子的检验,题目难度中等,注意将物质的性质与实际操作联系.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅 | B. | 硫 | C. | 铜 | D. | 铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ②③④ | C. | ①②③ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量为32g | B. | 含氧原子数为NA | ||
| C. | 含氧分子数为NA | D. | 在标准状况下,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
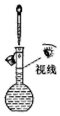
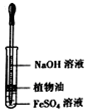
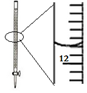
| A.配制0.10mol/L NaOH溶液 | B.观察Fe(OH)2的生成 | C.除去氯气中的氯化氢 | D.记录滴定终点读数为12.20mL |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别配成1mol/L的溶液,各取1mL滴加1滴酚酞试液,比较颜色深浅 | |
| B. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 | |
| C. | 分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀 | |
| D. | 分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色(必要时可透过蓝色钴玻璃) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸保存在无色玻璃试剂瓶中 | |
| B. | 氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 | |
| C. | 少量的钠保存在煤油或石蜡油中 | |
| D. | 新制的氯水通常保存在棕色玻璃试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com