
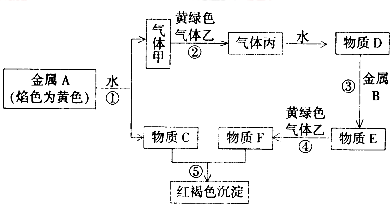
分析 金属A焰色反应为黄色,故A为Na,由反应①Na+水→气体甲+C,则甲为H2,C为NaOH,黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质D为盐酸.氢氧化钠与物质F反应生成红褐色沉淀是Fe(OH)3,故物质F中含有Fe3+,盐酸与金属B反应得到E,E与氯气反应得到F,可知金属B为Fe,物质E为FeCl2,物质F为FeCl3,据此解答.
解答 解:金属A焰色反应为黄色,故A为Na,由反应①Na+水→气体甲+C,则甲为H2,C为NaOH,黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质D为盐酸.氢氧化钠与物质F反应生成红褐色沉淀是Fe(OH)3,故物质F中含有Fe3+,盐酸与金属B反应得到E,E与氯气反应得到F,可知金属B为Fe,物质E为FeCl2,物质F为FeCl3.
(1)由上述分析可知,A为Na,丙为HCl,故答案为:Na;HCl;
(2)反应①的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,
反应④的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,
气体乙与C溶液反应离子方程式为:Cl2+2OH-+=Cl-+ClO-+H2O,
故答案为:2Na+2H2O═2Na++2OH-+H2↑;2Fe2++Cl2═2Fe3++2Cl-;Cl2+2OH-+=Cl-+ClO-+H2O;
(3)若将NaOH溶液与FeCl2溶液混合,则可以观察到的现象是:白色沉淀迅速变为灰绿色,最后变为红褐色,
故答案为:白色沉淀迅速变为灰绿色,最后变为红褐色;
(4)若将Na2O2投入到FeCl2溶液中,过氧化钠具有强氧化性,且与水反应生成氢氧化钠与氧气,可以观察到的现象是:有气体生成,有红褐色沉淀生成,
故答案为:有气体生成,有红褐色沉淀生成;
(5)为鉴定Fe单质,将试样溶于稀盐酸,取上层清液后需再加入KSCN溶液与氯水,开始无明显现象,加入氯水后溶液变为血红色,
故选:cd;
(6)向沸水中加入FeCl3饱和溶液,可制得一种红褐色液体,该液体是胶体的实验证明方法是:丁达尔效应,
故答案为:丁达尔效应.
点评 本题是考查无机物推断,焰色反应、物质的颜色与特殊反应是推断的突破口,掌握元素化合物的性质是解题的关键,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下0.1 mol•L-1的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,c(NH4+) 由大到小的顺序为②>①>③ | |
| B. | 常温下0.4 mol•L-1CH3COOH溶液和0.2 mol•L-1 NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.2 mol•L-1 NaHCO3溶液等体积混合所得溶液中:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) | |
| D. | 0.1 mol•L-1的氨水与0.05 mol•L-1 H2C2O4溶液等体积混合所得溶液中:c(NH4+)+c(NH3•H2O)=2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | bd | B. | bc | C. | ad | D. | 只有d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水中通入一定量的SO2气体可增强氯水的漂白性 | |
| B. | 因为SO2具有漂白性,所以它能使品红溶液、酸性高锰酸钾溶液褪色 | |
| C. | 已知酸性:H2SO4>HClO,则SO2通入漂白粉溶液中可生成次氯酸 | |
| D. | 紫色石蕊试液中通入SO2,溶液变红后不褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管 液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若保持温度,保持容器容积固定不变,向容器内补充B气体,则有a<b | |
| B. | 若保持温度、压强不变,充入惰性气体,则有a>b | |
| C. | 若其他条件不变,升高温度,则有a<b | |
| D. | 若a=b,则可能是在该温度下,保持容器容积固定不变情况下充入了惰性气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com